Журнал «Травма» Том 15, №5, 2014
Вернуться к номеру
Осложнения после эндопротезирования коленного сустава при использовании индивидуальных онкологических эндопротезов у больных с опухолями костей
Авторы: Проценко В.В., Дуда Б.С. - Государственное учреждение «Институт травматологии и ортопедии НАМН Украины», г. Киев
Рубрики: Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
В статье сделан анализ осложнений после эндопротезирования коленного сустава с использованием индивидуальных онкологических эндопротезов у 55 больных с опухолями костей. Основными осложнениями после эндопротезирования суставов были: асептическая нестабильность эндопротеза — у 10 (18,2 %) пациентов, парапротезная инфекция — у 7 (12,7 %), перелом конструкции эндопротеза — у 3 (5,4 %), перелом кости в месте имплантации эндопротеза — у 2 (3,6 %) больных. При асептической нестабильности эндопротеза и переломах конструкции эндопротеза 13 пациентам выполнено реэндопротезирование. Консервативное и хирургическое лечение по поводу парапротезной инфекции проведено 7 пациентам. При переломах кости в месте имплантации эндопротеза выполнен металлоостеосинтез кости накостными пластинами и проволочными серкляжами.
У статті зроблений аналіз ускладнень після ендопротезування колінного суглоба з використанням індивідуальних онкологічних ендопротезів у 55 хворих із пухлинами кісток. Основними ускладненнями після ендопротезування суглобів були: асептична нестабільність ендопротеза — у 10 (18,2 %) пацієнтів, парапротезна інфекція — у 7 (12,7 %), перелом конструкції ендопротеза — у 3 (5,4 %), перелом кістки в місці імплантації ендопротеза — у 2 (3,6 %) пацієнтів. При асептичній нестабільності ендопротеза і переломах конструкції ендопротеза 13 пацієнтам виконано реендопротезування. Консервативне та хірургічне лікування з приводу парапротезної інфекції проведено 7 пацієнтам. При переломах кістки в місці імплантації ендопротеза виконано металоостеосинтез кістки накістними пластинами і дротяними серкляжами.
This article analyzes complications after knee arthroplasty using individual cancer implants in 55 patients with bone tumors. Major complications after knee arthroplasty were: aseptic loosening of the endoprosthesis in 10 (18.2 %) patients, paraprosthetic infection in 7 (12.7 %) patients, fracture of the endoprosthesis in 3 (5.4 %) patients, bone fracture at the place of endoprosthesis implantation in 2 (3.6 %) patients. In cases of aseptic loosening of endoprosthesis and fracture of the endoprosthesis, 13 patients underwent revision of endoprosthesis. Conservative and surgical treatment for paraprosthetic infection was carried out in 7 patients. Osteosynthesis with the use of bone plates and wire cerclages was carried out in cases of bone fractures at the place of endoprosthesis implantation.
опухоли костей, коленный сустав, индивидуальное онкологическое эндопротезирование, послеоперационные осложнения, реэндопротезирование.
пухлини кісток, колінний суглоб, індивідуальне онкологічне ендопротезування, післяопераційні ускладнення, реендопротезування.
bone tumors, knee joint, individual cancer arthroplasty, postoperative complications, revision of endoprosthesis.
Статья опубликована на с. 70-74
Введение
Кости, образующие коленный сустав, в 60–70 % случаев поражаются злокачественными и доброкачественными опухолями [4]. Одним из видов хирургического лечения злокачественных и доброкачественных опухолей костей является эндопротезирование [14]. В современной онкоортопедии эндопротезирование возможно при поражении практически любого крупного сустава [1, 8]. Преимуществом эндопротезирования перед другими методами реконструкции является одномоментное замещение больших костных дефектов при сохранении движений в суставе, что обеспечивает хорошее восстановление функции и улучшение качества жизни больного [3]. Но вместе с тем эндопротезирование может вызывать осложнения, которые приводят к повторным операциям, в том числе к реэндопротезированию. Ревизионное эндопротезирование при первичном онкологическом эндопротезировании проводится приблизительно в 30 % случаев [12], а риск реэндопротезирования через пять лет составляет 12–32 %, через 10 лет — 25–61 % [11]. В литературе сообщается, что основными осложнениями после эндопротезирования являются: инфекционные осложнения, асептическая нестабильность эндопротеза, перелом конструкции эндопротеза, износ полиэтиленовых частей эндопротеза [6, 7]. Общая частота инфекционных осложнений после эндопротезирования крупных суставов у онкологических больных составляет 10 %, ранних — 57,6 %, отсроченных — 28,8 %, поздних — 13,6 % [2, 5, 9]. При локализации опухоли в дистальном отделе бедренной кости после эндопротезирования коленного сустава инфекционные осложнения возникают в среднем у 8 % больных, асептическая нестабильность — у 10 % и рецидивы — у 10 %, общий пятилетний срок службы эндопротеза составляет около 54 % [2, 5, 12, 15–17, 19]. При поражении проксимального отдела большеберцовой кости после эндопротезирования коленного сустава инфекционные осложнения возникают у 10–16 % больных, асептическая нестабильность — у 18 % и рецидивы — у 13 %, общий пятилетний срок службы эндопротеза составляет около 38 % [2, 5, 13, 18, 20]. Таким образом, осложнения после эндопротезирования суставов являются серьезной проблемой, которая ведет к нарушению функции, а иногда и к потере конечности, значительно ухудшает качество жизни больных, которым выполнено эндопротезирование сустава по поводу опухолей длинных трубчатых костей.
Материалы и методы
В клинических отделах ГУ «Институт травматологии и ортопедии НАМН Украины» за период с 2009 по 2013 год первичное эндопротезирование коленного сустава после удаления местноагрессивных и злокачественных опухолей было проведено 55 пациентам. 33 (60 %) из них были выполнены oпeрации эндопротезирования коленного сустава при резекции дистального отдела бедренной кости и 22 (40 %) — при резекции проксимального отдела большеберцовой кости. Мужчин было 32 (58,2 %), женщин — 23 (41,8 %), средний возраст пациентов составил 31,2 ± 1,2 года. Встречались следующие морфологические формы опухолей: гигантоклеточная опухоль кости — у 21 (38,2 %) пациента, остеогенная саркома (параостальная, периостальная, телеангиэктатическая, центральная, смешанная) — у 16 (29,1 %), хондросаркома — у 6 (10,9 %), фибросаркома — у 4 (7,3 %), злокачественная гигантоклеточная опухоль кости — у 4 (7,3 %), злокачественная фиброзная гистиоцитома кости — у 2 (3,6 %), лимфосаркома кости — у 1 (1,8 %), саркома Юинга — у 1 (1,8 %) пациента.
При эндопротезировании коленного сустава использованы эндопротезы следующих фирм: «Инмед» — 37 (67,3 %) случаев, Stryker — 15 (27,3 %), Link — 2 (3,6 %), «Безноска» — 1 (1,8 %).
Абластическое и радикальное удаление опухоли суставного сегмента кости обусловливало необходимость проведения обширной резекции. Длина резекции кости у пациентов была различной и составляла от 9 до 22 см. У 9 (16,4 %) больных рентгенологически и клинически до операции отмечался патологический перелом на фоне опухолевого поражения, что в немалой степени усложняло предоперационное обследование и создавало дополнительные технические сложности во время операции и при дальнейшей реабилитации. У 8 (14,5 %) больных наблюдался мягкотканный компонент опухоли. 6 (10,9 %) пациентам до проведения операции эндопротезирования по месту жительства были выполнены различные оперативные вмешательства (костно-пластические операции с использованием аутотрансплантатов и керамического материала на основе гидроксиапатита и трикальцийфосфата). 29 (52,7 %) пациентам в предоперационном периоде проводились курсы внутриартериальной или внутривенной полихимиотерапии. Из них 21 пациенту в предоперационном периоде делались внутривенные инфузии цисплатина, адриобластина, высокодозного ифосфамида и высокодозного метотрексата, 6 пациентам проводились внутриартериальные инфузии препаратов адриобластин и цисплатин и 2 больным — внутривенные инфузии адриобластина, цисплатина и высокодозного ифосфамида параллельно с лучевой терапией до суммарной очаговой дозы 30 Гр.
Анализ трехлетней выживаемости онкологического эндопротеза (усредненный срок службы имплантата) проводили при помощи F-теста Кокса.
Функциональный результат прооперированной конечности рассчитывался по шкале MSTS (Musculo — Sceletal Tumor Staging/System). Оценку качества жизни больных, которым сделано эндопротезирование сустава, проводили согласно опросу по системе EORTC QLQ-С30 (шкала баллов от 0 до 4). Выживаемость пациентов оценена методом Каплана — Мейера.
Полученные результаты и их обсуждение
После проведенного эндопротезирования коленного сустава у 55 больных нами получены следующие результаты: осложнения после эндопротезирования наблюдались у 22 (40 %) пациентов. Основными осложнениями были: асептическая нестабильность эндопротеза и его компонентов — у 10 (18,2 %) пациентов, парапротезная инфекция — у 7 (12,7 %), перелом металлической ножки эндопротеза и несостоятельность его узлов — у 3 (5,4 %), перелом кости в месте имплантации эндопротеза — у 2 (3,6 %). Рецидивы опухоли выявлены у 4 (7,2 %) пациентов. При лечении инфекционных осложнений в раннем послеоперационном периоде проводили хирургическое очищение раны и длительный курс антибиотикотерапии, в позднем — удаляли эндопротез и костный цемент, устанавливали цементный спейсер и проводили длительный курс антибиотикотерапии. Лечение инфекционных осложнений осуществляли у 7 пациентов: диализ и антибиотикотерапию — у 5, ревизионное реэндопротезирование — у 1, ампутацию конечности — у 1.
При асептическом расшатывании и несостоятельности узлов эндопротеза проведено реэндопротезирование у 13 (23,6 %) пациентов. 2 (3,6 %) пациентам с переломом кости в месте имплантации ножки эндопротеза выполнен металлоостеосинтез накостными пластинами и проволочными серкляжами.
У 3 (5,4 %) больных наблюдалось сочетание различных осложнений (нагноение и асептическое расшатывание или асептическое расшатывание и нагноение).
Локализация опухоли, по поводу которой выполнялось эндопротезирование сустава, также играла важную роль в возникновении осложнений. Проксимальная часть большеберцовой кости — более сложная локализация из-за недостаточности мягких тканей. Из 22 больных, которым были выполнены операции эндопротезирования коленного сустава после резекции проксимального отдела большеберцовой кости, осложнения наблюдались у 10 (45,5 %). У 5 (22,7 %) из них осложнением являлось парапротезное нагноение. У 4 (18,2 %) больных гнойно-воспалительные осложнения развивались в позднем послеоперационном периоде, в том числе в 2 случаях они развились на фоне расшатывания большеберцовой ножки эндопротеза. Из 33 больных, которым были выполнены операции эндопротезирования коленного сустава после резекции дистального отдела бедренной кости, осложнения наблюдались у 12 (36,4 %). У 2 (6,1 %) из них осложнением являлось парапротезное нагноение, в том числе в 1 случае оно развилось на фоне расшатывания бедренной ножки эндопротеза.
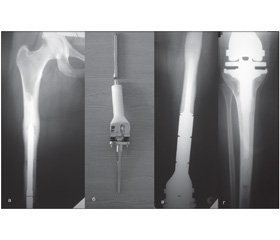
Случай из практики. Больная Ф. поступила в отделение с диагнозом: остеогенная саркома дистального отдела бедренной кости Т2N0M0, стадия II Б, клиническая группа II. После проведения четырех блоков внутривенной полихимиотерапии с использованием высокодозного метотрексата, доксорубицина и цисплатина и с учетом положительной клинико-рентгенологической динамики больной была выполнена резекция дистального отдела бедренной кости с опухолью и эндопротезирование коленного сустава эндопротезом фирмы «Безноска», в послеоперационном периоде больная получила еще 8 блоков внутривенной полихимиотерапии высокодозным метотрексатом и высокодозным ифосфамидом. Спустя 5 лет после физической нагрузки у пациентки произошел перелом бедренной ножки эндопротеза. Эндопротез был извлечен и произведено реэндопротезирование коленного сустава эндопротезом фирмы Stryker. В настоящее время каких-либо осложнений со стороны коленного сустава не наблюдается, пациентка передвигается самостоятельно, без вспомогательных средств.
Функциональный результат конечности после эндопротезирования по шкале MSTS составил 86 % после резекции дистального отдела бедренной кости и 78 % после резекции проксимального отдела большеберцовой кости. После реэндопротезирования при локализации дефекта в дистальном отделе бедренной кости трехлетняя выживаемость эндопротеза составила в среднем 80 %, функциональный результат конечности после реэндопротезирования по шкале MSTS равнялся в среднем 84 %. После реэндопротезирования при локализации дефекта в проксимальном отделе большеберцовой кости трехлетняя выживаемость эндопротеза составила в среднем 72 %, функциональный результат конечности после реэндопротезирования по шкале MSTS был равен в среднем 76 %.
Качество жизни пациентов после эндопротезирования коленного сустава (опросник EORTC QLQ-C30) повысилось с 45 до 80 баллов. Общая трехлетняя выживаемость пациентов составила 86,4 ± 0,12 %.
Заключение
Анализ полученных результатов показывает, что если до эндопротезирования сустава больным уже было выполнено какое-либо оперативное вмешательство, то это повышало риск возникновения послеоперационных осложнений. Асептическое расшатывание компонентов эндопротеза было обусловлено как техническими ошибками при эндопротезировании, так и использованием костного цемента и требовало ревизионной замены эндопротеза. Переломы конструкции эндопротеза обусловлены техническими погрешностями при его изготовлении.
При парапротезной инфекции с целью диагностики мы применяли обязательную пункцию сустава с аспирацией его содержимого и бактериальным исследованием, МРТ или КТ и радиоизотопное исследование. При лечении инфекционных осложнений учитывали, какая это инфекция: если ранняя (1 месяц после операции) — проводили хирургическое очищение раны, если поздняя (хроническая) — удаляли эндопротез и устанавливали металлоцементный спейсер, насыщенный антибиотиками, если гематогенная (поздняя, острое начало) — проводили хирургическое очищение раны, удаляли эндопротез и устанавливали металлоцементный спейсер, насыщенный антибиотиками, если интраоперационно была выявлена положительная культура возбудителя инфекции, проводили длительный курс антибиотикотерапии. При лечении осложнений эндопротезирования учитывали системные отягчающие факторы — хронические соматические заболевания и местные отягчающие факторы — множественные рассечения кожи, недостаточность кожных покровов, наличие свищевого хода, подкожные абсцессы более 8 см2, сосудистую недостаточность (отсутствие периферического пульса, венозный стаз), предшествующий периартикулярный перелом, облучение и химиотерапию, активно протекающую инфекцию. Учитывали также значительно отягчающие системные факторы: количество лейкоцитов меньше 1000, хроническую инфекцию иного органа или области поражения или опухоль иммунной системы.
Мы применяли стандартную лечебную тактику при нагноениях после эндопротезирования суставов, принятую классической хирургической и ортопедической школой: создание адекватного оттока из патологического очага, мощная антибактериальная терапия, максимальный покой пораженного органа, разгрузка и иммобилизация конечности. Проводились также альтернативные хирургические мероприятия в зависимости от стадии инфекционного процесса: хирургическое очищение раны, одномоментная замена эндопротеза, двухмоментная замена эндопротеза с применением металлоцементного спейсера, удаление эндопротеза и создание артродеза, ампутация (экзартикуляция) конечности.
Полученные удовлетворительные функциональные результаты реэндопротезирования коленного сустава говорят о необходимости выполнения этой операции как альтернативной методики лечения осложнений эндопротезирования.
Выводы
1. Осложнения после эндопротезирования, как правило, связаны с асептикой и антисептикой во время операции, дефектами конструкций эндопротезов и техники проведения оперативных вмешательств.
2. При реэндопротезировании требуется выполнение всех мероприятий в полном объеме, с учетом всех факторов, которые привели к осложнениям, что позволяет сохранить не только конечность, но также ее функцию и опороспособность и таким образом повысить качество жизни данной категории больных.
1. Алиев М.Д. Эндопротезирование как основа онкоортопедии / М.Д. Алиев // Поволжский онкологический вестник. — 2012. — № 2. — С. 14-20.
2. Амирасланов А.О. Эндопротезирование крупных костей и суставов у онкологических больных: Автореф. дис… д-ра мед. наук. — М., 2007.
3. Балберкин А.В. Клиника, диагностика и хирургическое лечение опухолей костей области коленного сустава / А.В. Балберкин, Д.А. Шавырин // Саркомы костей, мягких тканей и опухоли кожи. — 2013. — № 1. — С. 15-23.
4. Дедков А.Г. Эндопротезирование коленного сустава при новообразованиях костей, его образующих / А.Г. Дедков, В.В. Проценко // Вісник ортопедії, травматології та протезування. — 2009. — № 2 (61). — С. 36-40.
5. Несиченко Д.В. Инфекционные осложнения у онкологических больных после эндопротезирования крупних суставов. Клиника, диагностика, лечение, профилактика: Автореф. дис… канд. мед. наук. — М., 2010.
6. Проценко В.В. Ускладнення після ендопротезування суглобів у хворих на пухлини довгих кісток / В.В. Проценко // Галицький лікарський вісник — 2009. — Т. 16, № 3. — С. 56-59.
7. Фитцек И. Двухэтапная ревизия со сменой протеза коленного сустава и применением артикулирующего спейсера в лечении околопротезной инфекции / И. Фитцек, В. Горбачев // Проблема эндопротезирования лучезапястного, коленного и голеностопного суставов: Тезисы докладов международной конференции. — М., 2001. — С. 13-14.
8. Эндопротезирование при опухолевом поражении длинных костей / В.В. Тепляков, В.Ю. Карпенко, Г.А. Франк и др. // Российский педиатрический журнал. — 2009. — № 5. — С. 11-14.
9. Wodajo F.M., Bickels J., Wittig J. [et al.] Complex reconstruction in the management of extremity sarcomas // Curr. Opin. Oncol. — 2003. — Vol. 15. — P. 304-312.
10. Bickels J., Wittig J.C., Kollender Y. [et al.] Distal femur resection with endoprosthetic reconstruction: a long-term followup study // Clin. Orthop. — 2002. — Vol. 400. — P. 225-235.
11. Myers G.J., Abudu A.T., Carter S.R. [et al.] Endoprosthetic replacement of the distal femur for bone tumours: long-term result // Bone Jount Surg. Br. — 2007. — Vol. 89 (4). — P. 521-526.
12. Henderson E.R., Jogn S., Groundiand J.S. [et al.] Failure mode classification for tumor endoprostheses: retrospective review of five institutions and a literature review // J. Bone Jount Surg. Am. — 2011. — Vol. 93. — P. 418-429.
13. Henshaw R.M., Jones V., Malawer M.M. Endoprosthetic reconstruction with the modular replacement system // Fourth annual combined meeting of the American and European Musculoskeletal Tumor Societies. — Washington, 1998. — P. 34-67.
14. Malawer M.M. Prosthetic survival and clinic results with use of lorge-segment replacement in the treatment of high-grade bone sarcomas / M.M. Malawer, L.B. Chou // J. Bone Jount Surg. — 1995. — Vol. 77. — P. 1154-1165.
15. Malawer M.M. Distal femoral resection for sarcomas of bone // Musculoskeletal surgery for cancer / Ed. by P.H. Sugarbaker, M.M. Malawer. — New York: Thieme Medical Publishers, 1992. — P. 43-259.
16. Biau D., Faure E., Katsahian S. [et al.] Survival of total knee replacement with a megaprosthesis after bone tumor resection // J. Bone Jount Surg. Am. — 2006. — Vol. 88 (6). — P. 85-93.
17. Peabody T.D., Eckardt J.J. Complication of prosthetic reconstruction // Surgery for bone and soft-tissue tumors / M.A. Simon, D. Springfield. — Philadelphia: J.B. Lippincott-Raven, 1998. — P. 467-479.
18. Jacob B., James C., Kollender Y. [et al.] Reconstruction of the extensor mechanism after proximal tibia endoprosthetic replacement // J. Arthroplasty. — 2001. — Vol. 16 (7). — P. 28-43.
19. Unwin P.S. Aseptic loosening in cemented custom megaprosthesis for malignant bone tumours of lower limb / P.S. Unwin, S.R. Cannon, R.J. Grimer // J. Bone Jount Surg. (Br.) — 1996. — Vol. 78 (1). — P. 5-13.
20. Zachary A. Proximal tibia resection and prosthetic reconstruction / A. Zachary, R.H. Quinn // Techn. Orthop. — 2007. — Vol. 22 (2). — P. 88-98.

/72/72.jpg)