Журнал «Травма» Том 12, №4, 2011
Вернуться к номеру
Мультипотентні мезенхімальні стромальні клітини кісткового мозку в лікуванні діафізарних переломів
Авторы: Шимон В.М., Шерегій А.А., Ужгородський національний університет, медичний факультет, кафедра загальної хірургії з курсами травматології і ортопедії, оперативної хірургії та судової медицини
Рубрики: Травматология и ортопедия
Версия для печати
За результатами проведеного аналізу пролікованих за період 2008–2010 рр. в умовах клініки ортопедії ЗОКЛ ім. А. Новака 168 пацієнтів з приводу діафізарних переломів довгих кісток та 34 пацієнтів із наслідками травми отримано переконливі дані щодо доцільності використання трансплантації мультипотентних мезенхімальних стромальних клітин кісткового мозку в кістковий дефект з метою стимуляції репаративного остеогенезу.
Діафізарні переломи, репаративний остеогенез, мультипотентні мезенхімальні стромальні клітини кісткового мозку.
Вступ
Проблема лікування хворих із переломами довгих кісток кінцівок завжди була та є актуальною, займаючи провідне місце в структурі загального травматизму як в Україні, так і на Заході. Частота діафізарних переломів сягає до 48,5 % випадків усіх переломів довгих кісток кінцівок, серед них переломи стегнової кістки становлять 11,27 %, гомілки — до 28 %, та є однією з основних причин тривалої тимчасової непрацездатності та первинної інвалідності у хворих після травм і хвороб опорно-рухового апарату [3, 5]. В Україні у структурі оперативних втручань 65,8 % займають традиційні оперативні втручання й методики остеосинтезу (накісткові пластини, апарати позавогнищевої фіксації, інтрамедулярний остеосинтез). Досвід застосування сучасних малоінвазивних методик остеосинтезу при переломах довгих кісток, яким віддають перевагу лише у 4,7 %, вказує на те, що розробкою та вдосконаленням фіксаторів достеменно вирішити проблему кісткової регенерації не вдається. Ряд питань, пов’язаних з так званою остеогенною недостатністю, залишається невирішеним [3, 4, 6, 9].
У зв’язку з цим пошук та забезпечення найбільш оптимальних умов перебігу репаративно-регенераторних процесів при порушенні цілісності кісткової тканини визначено як перспективний та пріоритетний напрямок наукових досліджень нового тисячоліття. На сьогодні з метою активізації репаративного остеогенезу при багатоуламкових переломах та переломах з дефектом тканин використовують синтетичні кальцій-фосфатні біоматеріали у вигляді кераміки або композитів [1, 2, 7, 13]. Найчастіше для кісткової пластики, зокрема при лікуванні сповільненої консолідації кісткових уламків та псевдоартрозів, використовують губчасту кісткову тканину хворого, яку вважають золотим стандартом серед різних пластичних матеріалів. Цей метод відрізняється від інших кондуктивною й остеогенною активністю за рахунок стовбурових клітин кісткового мозку та ендосту. Недоліком способу є нанесення додаткової операційної травми, збільшення крововтрати та часу самого оперативного втручання, відповідно й анестезії.
Натепер активно розвивається новий напрям регенераторної медицини — клітинна та тканинна інженерія [10–12]. Клітинні технології включають в себе розробку методів отримання клітинних культур, оцінку їхнього впливу на репаративний остеогенез, а також технології їх застосування в практичній медицині.
Мета дослідження — проаналізувати результати лікування діафізарних переломів при трансплантації мультипотентних мезенхімальних стромальних клітин кісткового мозку в зону перелому.
Матеріали та методи
За період 2008–2010 рр. в умовах клініки ортопедії ЗОКЛ ім. А. Новака з приводу діафізарних переломів довгих кісток госпіталізовано 168 пацієнтів. Пацієнтів, які звернулися з приводу ускладнень, незадовільних результатів попереднього лікування переломів, об’єднали в окрему групу (34 особи).
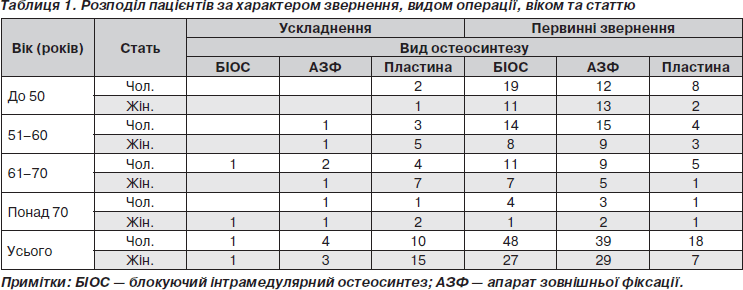
Хворі були розподілені таким чином: пацієнти, які звернулися з приводу травми, віднесені до основної групи (168 осіб); серед них пацієнтів, які звернулися з приводу ускладнень та незадовільних результатів, було 34. У кожній з цих груп сформовано підгрупи за такими критеріями: за статтю — 105 чоловіків, 63 жінки; група з ускладненнями — 15 чоловіків, 19 жінок; 4 вікові групи: до 50 років — 41 чоловік та 27 жінок; 51–60 років — 37 чоловіків та 26 жінок, 61–70 років — 32 чоловіки та 21 жінка; понад 71 рік — 10 чоловіків та 8 жінок (табл. 1). Контрольні огляди проводили в термін 2, 4, 6 міс. та 12 місяців за можливості.
З метою застосування найбільш адекватного методу оперативного лікування переломів за показаннями застосовували різні методики оперативних втручань, а саме: позавогнищевий остеосинтез апаратами зовнішньої фіксації, інтрамедулярний остеосинтез, погружний накістковий остеосинтез, у тому числі пластини з кутовою стабільністю, та консервативну терапію. Під часні передопераційної підготовки використовували системи скелетного витяжіння у 37 (22,1 %) випадках первинних звернень.
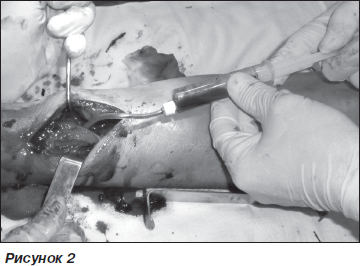
У 6 випадках при переломах гомілки, у 5 випадках при переломах стегнової кістки та в 1 випадку при переломі плечової кістки використовували АЗФ. З метою покращення прогностичних очікувань застосовували кісткову автопластику в зоні дефекту, культивувавши суміш мезенхімальних клітин кісткового мозку (рис. 1), отриману з просвіту інтрамедулярного каналу на 3–5 см вище або нижче від лінії перелому, залежно від наближеності перелому до епіфізу кістки (рис. 2) у 137 випадках при гострій травмі та у 34 випадках при повторних операціях. При застосуванні позавогнищевої фіксації уламків у 25 випадках при заміні методу через незрощення та в 11 випадках, де був виконаний перемонтаж апарату зовнішньої фіксації, матеріал кісткового мозку отримували пункційно з найбільш наближеного до метафізу трепанаційного отвору кістки для проведення стрижнів апарату зовнішньої фіксації та вводили черезшкірно в зону перелому після репозиції та остаточної фіксації. У разі інтрамедулярного остеосинтезу кістковий мозок отримували з отвору для введення стрижня пункційним методом та вводили черезшкірно при закритій репозиції або вільно при відкритій репозиції після блокування стрижня гвинтами.

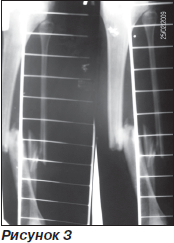
На контрольних рентгенограмах до операції (рис. 3), після операції (рис. 4) та через 2 місяці після операції (рис. 5) візуалізуються ознаки консолідації перелому.


Результати та обговорення
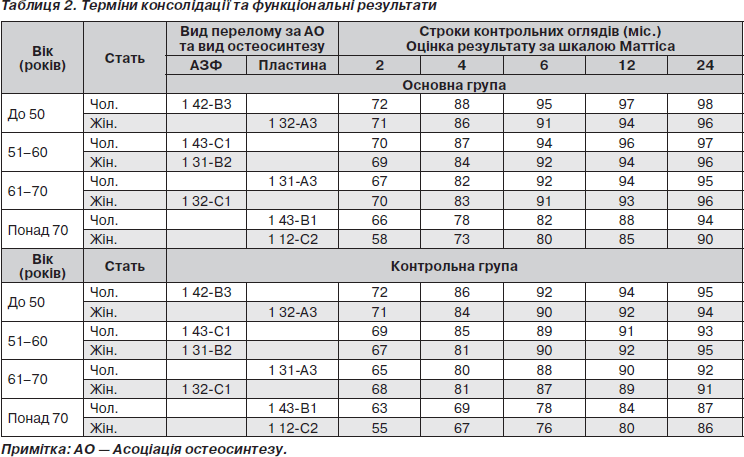
Результати лікування оцінювали відповідно до критеріїв R. Johner, O. Wruhs [9] за допомогою рентгенологічного обстеження, за даними об’єктивного спостереження, відновленням функції кінцівки та її здатністю витримувати тривале навантаження. З метою порівняльного аналізу оцінкам «відмінно», «добре», «задовільно» та «незадовільно» присвоєні кількісні значення — 5, 4, 3, 2 відповідно. З метою оцінки функціональних результатів лікування використовували 100-бальну шкалу Маттіса (табл. 2) [8].
У термін 2 місяці після операції відхилень від очікуваних результатів відзначено не було, у 4 місяці післяопераційного періоду повторно було оглянуто 182 пацієнти, результати були розцінені як відмінні у 89 %, добрі — у 5 % та задовільні — у 6 %. За 6 місяців оглянуто 139 пацієнтів. Результати розцінені як відмінні у 81 %, добрі — у 9 %, задовільні — у 7 % та незадовільні — у 3 %. За 12 місяців оглянуто 107 пацієнтів. Результати були такі: відмінні — у 80 %, добрі — у 10 %, задовільні — у 6 %, незадовільні — у 4 %.
Як видно з наведеної табл. 2, найбільше число ускладнень при остеосинтезі діафізарних переломів має метод накісткового остеосинтезу — 25 випадків (73,5 % серед усіх незадовільних результатів). Аналізуючи наведені дані, слід відзначити, що більша частина пацієнтів — це жінки, які народили двох або більше дітей (7 хворих).
Після застосування черезкісткового остеосинтезу незадовільні результати були у 7 (20,5 %) випадках. У 2 (5,8 %) випадках спостерігався незадовільний результат після блокуючого інтрамедулярного остеосинтезу у вигляді незрощення перелому.
Пацієнти, які надходили з незадовільними результатами попереднього лікування, були повторно оперовані в умовах клініки ортопедії і травматології ЗОКЛ ім. А. Новака. У даній групі пацієнтів (17 випадків) було здійснено блокуючий інтрамедулярний остеосинтез без розсвердлювання інтрамедулярного каналу; римеризація застосовувалась у 6 випадках. Апарат зовнішньої фіксації застосовувався в 11 випадках. Усі оперативні втручання доповнювалися кістковою автопластикою матеріалом кісткового мозку з епіфізів оперованої кістки в зоні перелому.
З метою наочності було сформовано контрольну групу пацієнтів (30 осіб) із подібними свіжими переломами, у яких оперативні втручання не доповнювалися кістковою автопластикою. В основну групу увійшли пацієнти (137 осіб), яким під час оперативного втручання здійснювали кісткову автопластику за вищеописаною методикою. Оцінювали рентгенологічну картину кісткового регенерату, функціональний результат, об’єктивні дані локального статусу, суб’єктивну картину.
Як видно з табл. 2, у пацієнтів, яким було виконано кісткову автопластику матеріалом кісткового мозку з кістково-мозкового каналу, рентгенологічно та клінічно зрощення наступало раніше, ніж у пацієнтів контрольної групи, що, в свою чергу, дає підставу для розширення показань до цього етапу під час оперативних втручань з приводу діафізарних переломів.
Висновки
Трансплантація мультипотентних мезенхімальних стромальних клітин кісткового мозку в кістковий дефект стимулює репаративний остеогенез.
Розширення показань до кісткової автопластики отриманим пункційно матеріалом кісткового мозку при багатоуламкових переломах, поєднаних з великими дефектами кістки, після резекції новоутворень тощо, дає змогу збільшити питому вагу добрих результатів та зменшити час тимчасової непрацездатності.
Дана методика потребує подальшого вивчення та вдосконалення.
Волков А.В. Тканевая инженерия: новые перспективы развития медицины / А.В. Волков // Клеточная трансплантология и тканевая инженерия. — 2005. — № 1. — С. 57-63.
Дєдух Н.В. Регенерація кістки: досягнення та перспективи / Н.В. Дєдух, С.В. Малишкіна // Травма. — 2006. — Т. 7, № 2. — С. 212-216.
Гайко Г.В. Діафізарні переломи в структурі травм опорно-рухової системи у населення України / Г.В. Гайко, А.В. Калашніков, В.А. Боєр та ін. // Вісн. ортопед., травматол. та протезування. — 2006. — № 1. — С. 84-87.
Деев Р.В. Клеточные технологии в травматологии и ортопедии / Р.В. Деев, А.А. Исаев, А.Ю. Кочиш, P.M. Тихолов // Травматология и ортопедия России. — 2007. — Вып. 46. — № 4. — С. 18-30.
Кесян Г.А., Берченко Г.Н., Уразгильдеев Р.З., Микелаишвили Д.С., Арсеньев И.Г. и др. Применение отечественного препарата Коллапан в комплексном лечении переломов и ложных суставов длинных трубчатых костей // Применение искусственного имплантата Коллапан в травматологии и ортопедии. — М., 2008. — С. 16-18.
Корж Н.А. Репаративная регенерация кости: современный взгляд на проблему. Стадии регенерации (сообщение 1) / Н.А. Корж, Н.В. Дедух // Ортопедия, травматология и протезирование. — 2006. — № 1. — С. 77-84.
Корж Н.А. Репаративная регенерация кости: современный взгляд на проблему. Методы тканевой терапии и генной инженерии (сообщение 6) / Н.А. Корж, Н.В. Дедух, Н.А. Ашукина // Ортопедия, травматология и протезирование. — 2006. — № 3. — С. 93-99.
Маттис Э.Р. Система оценки исходов переломов костей опорно-двигательного аппарата и их последствий: Автореф. дис... д-ра мед. наук: 14.00.22. — М., 1985. — 25 с.
Шимон В.М. Перспективні напрями лікування діафізарних переломів кісток гомілки / В.М. Шимон, А.А. Шерегій // Травма. — 2010. — Т. 11, № 4. — С. 363-366.
Krebsbach P.H. Dental and Skeletal Stem Cells: Potential Cellular Therapeutics for Craniofacial Regeneration / P.H. Krebsbach, P.G. Robey // J. Dent. Edu. — 2002. — Vol. 66, № 6. — P. 766-773.
Langer R. Tissue engineering / R. Langer, J.P. Vacanti // Science. — 1993. — Vol. 260, № 5110. — P. 920-926.
Mankani M.H. In vivo bone formation by Human marrow stromal cells: Reconstruction of the mouse calvarium and mandible / M.H. Mankani, S.A. Kuznetsov, R.M. Wolfe et al. // Stem. cells. — Vol. 24, № 9. — P. 2140-2149.
Ohgushi H. Osteogenic differentiation of cultured marrow stromal stem cells on the surface of bioactive glass ceramics / H. Ohgushi, Y. Dohi, T. Yoshikawa, S. Tamai et al. // J. Biomed. Mater. Res. — 1996. — Vol. 32, № 30. — P. 341-348.