Журнал «Травма» Том 12, №4, 2011
Вернуться к номеру
Сравнение эффективности и безопасности декскетопрофена трометамола и кетопрофена при их внутривенном введении с целью обезболивания после ортопедических вмешательств
Авторы: Zippel H., Wagenitz A., Department of Orthopaedics, Charite-University Medicine, Berlin, Germany
Рубрики: Травматология и ортопедия
Версия для печати
Цель настоящего исследования сводилась к тому, чтобы оценить обезболивающую эффективность и безопасность декскетопрофена трометамола, нестероидного противовоспалительного средства, по сравнению с его исходным рацемическим соединением кетопрофеном (оба препарата вводили внутривенно) у пациентов с послеоперационной болью.
Методы. Дизайн исследования носил многоцентровой рандомизированный двойной слепой параллельно-групповой характер. В общей сложности 252 пациента с умеренной и тяжелой болью после протезирования тазобедренного или коленного сустава, выполненного в условиях общей анестезии, были случайно распределены к получению декскетопрофена трометамола в дозе 50 мг или кетопрофена в дозе 100 мг. Оба препарата вводили внутривенно каждые 8 ч в течение 2 дней. Пациентов включали в исследование лишь в том случае, если интенсивность боли по 100-мм визуальной аналоговой шкале (ВАШ) была ≥ 40 мм. В ходе исследования была оценена интенсивность боли по ВАШ в разные отрезки времени после введения первой дозы тестируемых препаратов, после чего в качестве первичной переменной эффективности была рассчитана сумма разниц интенсивности боли (СРИБВ0–8 ч). Кроме того, была оценена необходимость в применении резервных обезболивающих средств, максимальная разница интенсивности боли (РИБmax), время до достижения РИБmax и безопасность применения тестируемых средств.
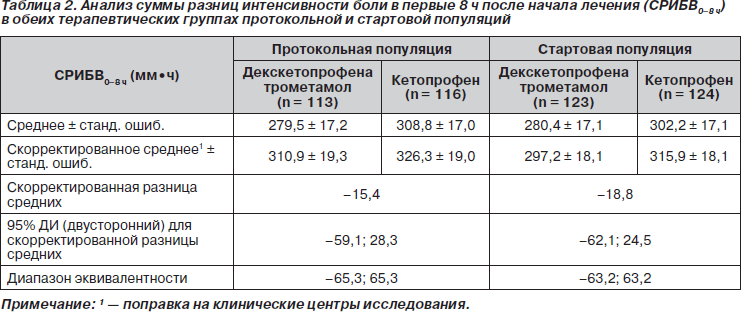
Результаты. Средние (± станд. ошиб.) скорригированные значения СРИБВ0–8 ч в протокольной популяции составили 310,9 ± 19,2 и 326,3 ± 19,0 мм•ч в группах с декскетопрофена трометамолом и кетопрофеном соответственно. 95% доверительный интервал для разницы между обоими видами терапии (от –59,1 до 28,3) полностью находился в пределах диапазона эквивалентности (± 65,3 мм•ч). В ходе исследования не было обнаружено достоверных различий в отношении вторичных переменных. Необходимость в применении резервных обезболивающих средств оказалась высокой в обеих группах — у 81,3 % пациентов из группы с декскетопрофена трометамолом и у 87,1 % пациентов из группы с кетопрофеном. Время до достижения РИБmax после введения декскетопрофена трометамола и кетопрофена составило 284,7 и 308,5 мин соответственно. Побочные эффекты, непосредственно связанные с приемом тестируемых препаратов, наблюдались у 16 % пациентов из группы с декскетопрофена трометамолом и у 21,3 % — с кетопрофеном. Большая часть пациентов получала сопутствующую терапию низкомолекулярными гепаринами (94,4 %), при этом не было отмечено каких-либо геморрагических осложнений, связанных с перенесенной операцией. В ходе исследования не наблюдалось побочных эффектов, отражающих нарушение функции почек.
Выводы. Оба тестируемых препарата были эквивалентны по обезболивающей активности при лечении послеоперационной боли после ортопедических вмешательств. Высокая частота использования резервных обезболивающих средств свидетельствует о необходимости применения мультимодального подхода к обезболиванию после данного типа операций. В ходе исследования была обнаружена тенденция к более лучшей переносимости декскетопрофена трометамола по сравнению с кетопрофеном.
Трометамол, кетопрофен, боль после ортопедического вмешательства, анальгезия, интенсивность боли, параллельно-групповое мультицентровое двойное слепое клиническое исследование.
Введение
Нестероидные противовоспалительные средства (НПВС) представляют собой структурно гетерогенную группу веществ с обезболивающей, жаропонижающей и противовоспалительной активностью. Считается, что первичный механизм действия этих средств связан с ингибированием ферментов семейства циклооксигеназ (ЦОГ), которые вовлечены в биосинтез простагландинов [1, 2]. Кетопрофен является членом арилпропионатной группы НПВС и обладает хорошо изученными обезболивающими и противовоспалительными эффектами [3, 4]. Он представляет собой рацемическое соединение, состоящее из смеси двух его энантиомеров в соотношении 50 : 50. Как и в отношении других производных арилпропионовой кислоты, было показано, что ингибиторные эффекты кетопрофена в отношении изоферментов ЦОГ-1 и ЦОГ-2 связаны с его S(+)-энантиомером (декскетопрофен), в то время как его левовращающий энантиомер, R(–)-кетопрофен, лишен подобной активности [5].
Разработка декскетопрофена, чистого S(+)-энантиомера кетопрофена, отражает современную тенденцию замены рацемических препаратов их энантиомерически чистыми формами, что способствует снижению дозы препарата, требуемой для достижения необходимого терапевтического эффекта, и снижению частоты развития побочных эффектов [5, 6]. Декскетопрофен был разработан в виде водорастворимой трометаминовой соли (декскетопрофена трометамол) и доступен как в виде обычных таблеток (с быстрым высвобождением вещества) в дозе 12,5 и 25 мг, так и в виде растворов для парентеральных инъекций (эта форма появилась на рынке недавно). Фармакокинетические исследования свидетельствуют о том, что декскетопрофена трометамол быстро и полностью абсорбируется после перорального приема и что его максимальная концентрация в плазме крови достигается значительно быстрее, чем у кислых форм декскетопрофена и кетопрофена, что значительно увеличивает его пригодность для лечения боли [7]. В ряде клинических исследований, в ходе которых пациентам с острой и хронической болью назначали декскетопрофена трометамол перорально, были подтверждены высокая обезболивающая эффективность и хороший профиль переносимости данного препарата [8–10]. В более ранних исследованиях также была оценена обезболивающая эффективность пероральной формы декскетопрофена трометамола по сравнению с энантиомерически эквивалентными дозами рацемического соединения кетопрофен [10–12]. У пациентов с зубной болью декскетопрофен обладал такой же обезболивающей эффективностью, как и кетопрофен, однако имел более быстрое начало действия [10]. Аналогичные результаты были получены и в исследовании, выполненном у женщин с первичной дисменореей [11].
Не так давно появилась новая форма декскетопрофена трометамола — для парентерального введения (внутримышечного и внутривенного), которая обладает хорошей обезболивающей активностью и хорошим профилем безопасности при различных видах острой боли, например при послеоперационной боли и почечной колике [13, 14]. Одним из преимуществ использования НПВС при послеоперационной боли является возможность их назначения в комбинации с опиоидами. Подобный подход уменьшает потребление опиоидов, что приводит к снижению риска угнетения дыхания, снижению седации, улучшению подвижности и взаимодействия, более быстрому восстановлению функции кишечника, снижению частоты послеоперационной тошноты и рвоты [15].
Стоит отметить, что по состоянию на сегодняшний день не было выполнено исследований, в ходе которых оценивалась бы обезболивающая эффективность декскетопрофена трометамола по сравнению с кетопрофеном при их внутривенном введении пациентам с острой послеоперационной болью. Ранее было показано, что внутривенное введение кетопрофена обеспечивает более эффективную анальгезию и приводит к снижению потребности в резервных обезболивающих средствах по сравнению с плацебо у пациентов после протезирования тазобедренного или коленного сустава [16]. Этот факт позволяет выполнить исследование эквивалентности, в ходе которого будут прямо сравниваться кетопрофен и декскетопрофена трометамол, без необходимости включения в исследование плацебо-группы.
Таким образом, первичная цель настоящего исследования сводилась к тому, чтобы оценить обезболивающую эффективность декскетопрофена трометамола по сравнению с кетопрофеном при их внутривенном введении через каждые 8 ч в течение 2 дней у пациентов с умеренной и тяжелой послеоперационной болью после протезирования коленного или тазобедренного сустава.
Методы
Дизайн исследования
Настоящее рандомизированное двойное слепое параллельно-групповое исследование было выполнено на базе 11 клинических центров интенсивной терапии в четырех странах (Бельгия, Франция, Германия и Южно-Африканская Республика). Исследование было проведено в соответствии с Хельсинской декларацией и одобрено комиссиями по биоэтике в каждом из клинических центров. Все пациенты дали письменное информированное согласие на участие в исследовании. Пациентов включали в наблюдение в период с 27 января 1999 г. по 5 августа 1999 г.
Критерии включения в исследование
В исследование включали пациентов в возрасте 18–75 лет, сообщавших о наличии умеренной или тяжелой боли (интенсивность боли ≥ 40 мм по 100-мм визуальной аналоговой шкале (ВАШ)) в течение первых 12 ч после выхода из общей анестезии (наркоз давали по стандартной схеме, наработанной в каждом из клинических центров) после элективного одностороннего протезирования тазобедренного или коленного сустава. У пациентов не должно было быть других видов боли, которые могли бы нарушать количественную оценку послеоперационной боли. Они должны были быть способны правильно пользоваться шкалами для оценки интенсивности боли и часами. У них не должно было быть противопоказаний к приему тестируемых препаратов или резервных обезболивающих средств (морфин, парацетамол (ацетаминофен) или пропацетамол).
Критерии исключения пациентов из исследования: повышенный риск послеоперационной гиповолемии вследствие высокой периоперационной кровопотери; гиперчувствительность или непереносимость кетопрофена, декскетопрофена трометамола, морфина, парацетамола или других НПВС; наличие в анамнезе астмы, клинически значимых заболеваний сердца, почек или печени, активной язвы желудочно-кишечного тракта или воспалительной болезни кишечника, кровотечения или гематологических нарушений, повышенного внутричерепного давления или судорог, наркотической или алкогольной зависимости; наличие любого клинически значимого нарушения, которое могло бы влиять на метаболизм или экскрецию тестируемых препаратов; высокий риск тромбоза глубоких вен; использование седативных средств, транквилизаторов или анксиолитиков, за исключением низких доз пероральных снотворных, принимаемых на ночь; прием препаратов, которые, как принято считать, могут обеспечивать анальгезию (например, кофеин или антигистаминные средства), в течение 3 ч до назначения тестируемых препаратов; применение НПВС в течение 12 ч до операции (24 ч для длительно действующих НПВС) или любого обезболивающего средства в течение 12 ч до назначения тестируемых препаратов (за исключением фентанила, вводимого во время операции); использование антикоагулянтов в течение последнего месяца (за исключением стандартных антикоагулянтов в низких дозах для профилактики тромбоза глубоких вен); применение ингибиторов моноаминоксидазы, барбитуратов (за исключением тиопентала, назначаемого в качестве вводного наркоза), изониазида, пробенецида, противоэпилептических средств или зидовудина; применение метотрексата или лития в течение 24 ч до выполнения операции; участие в других клинических исследованиях в течение предшествующих 30 дней. Беременные женщины, кормящие матери и женщины фертильного возраста, не использующие адекватные методы контрацепции, также были исключены из исследования.
Тестируемые препараты
В течение первых 12 ч после выхода из общей анестезии пациентов, соответствующих критериям включения в исследование, «слепо» распределяли в соответствии со схемой рандомизации, предварительно сформированной компьютером, к получению фиксированной дозы того или иного тестируемого препарата. Рандомизацию выполняли в блоках по четыре пациента. Назначенная терапия включала либо декскетопрофена трометамол в дозе 150 мг/день (выполняли 30-минутную инфузию 50 мг декскетопрофена трометамола, разведенного в 100 мл физиологического раствора, 3 раза в день) в течение 2 дней, либо кетопрофен в дозе 300 мг/день (выполняли 30-минутную инфузию 100 мг кетопрофена, разведенного в 100 мл физиологического раствора, 3 раза в день) в течение 2 дней. Инфузаты готовили не ранее чем за 3 ч до введения. До приготовления инфузатов тестируемые препараты были различимы по внешнему виду. Поэтому для сохранения «слепости» исследования инфузаты приготавливал человек, которой не был причастен к оценке пациентов.
Пациентам, у которых наблюдалось недостаточное ослабление боли после первого введения тестируемого препарата, могли быть назначены резервные обезболивающие средства. К ним относили морфин, назначаемый в дозе 10 мг (только парентерально) до максимальной дневной дозы 30 мг, парацетамол (любая лекарственная форма) до максимальной дневной дозы 3 г или пропацетамол до максимальной дневной дозы 6 г. Тех пациентов, которым назначали резервные обезболивающие средства в течение первого получаса терапии, исключали из исследования. Применения специальной техники, позволяющей пациенту самому контролировать введение морфина, не допускалось.
Оценка клинических показателей
Нулевое время (Т0) было определено как начало первой инфузии тестируемого препарата. Инфузии тестируемого препарата выполняли через каждые 8 ч в следующих точках времени: Т0, 8 ч (Т8), 16 ч (Т16), 24 ч (Т24), 32 ч (Т32) и 40 ч (Т40). Оценку интенсивности боли (по 100-мм ВАШ) выполняли спустя 15 и 30 мин после первого введения тестируемого препарата, а также спустя 1, 2, 4, 6, 8, 16, 24, 32, 40 и 48 ч. Интенсивность боли в Т8, Т16, Т24, Т32 и Т40 оценивали непосредственно перед введением тестируемого препарата. Оценку жизненно важных показателей (артериальное давление и частота сердечных сокращений в положении лежа) выполняли во время фазы скрининга, перед Т0 и в Т48. Лабораторные тесты (гематологические, биохимический профиль и анализ мочи) проводили во время скрининга, а также в Т48 или Т72. Если в Т48 или Т72 обнаруживались клинически значимые нарушения, то жизненно важные показатели и лабораторные тесты оценивали повторно на 7-й день (± 2 дня).
Переносимость
Информация о развитии побочных эффектов собиралась на основе спонтанных сообщений пациентов, а также путем общего опроса пациентов (не наталкивающего их на конкретную жалобу) в различные точки времени (в те же самые, когда оценивали интенсивность боли). К побочным эффектам относили также признаки и симптомы, наблюдаемые исследователями, а также клинически значимые нарушения лабораторных показателей. Регистрировали время появления, длительность и выраженность побочных эффектов. Последнюю определяли на основе субъективной оценки пациентов и классифицировали как легкую (признаки и симптомы легко переносились), умеренную (появившийся дискомфорт влиял на нормальную активность пациентов) или тяжелую (невозможно выполнять повседневные действия). Исследователь оценивал связь между приемом тестируемого препарата и наблюдаемым побочным эффектом (ее классифицировали как неизвестную, отдаленную, возможную, вероятную или как ту, которую невозможно оценить). В дополнение к этому пациенты должны были сообщать о развитии любых побочных эффектов, которые появлялись в течение 10 дней после окончания исследования, по телефону.
Оценка эффективности лечения
В качестве первичной переменной эффективности служила сумма разниц интенсивности боли (РИБ) за первые 8 ч после начала лечения, взвешенная по времени, прошедшему между наблюдениями (СРИБВ0–8 ч).
РИБ рассчитывали для каждой точки времени по следующей формуле:
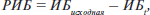
где ИБ — это интенсивность боли.
Эффективность терапии за 8 ч лечения определяли по следующей формуле:

Значения ВАШ, которые не были измерены вследствие того, что больные заснули, заменили нулевыми значениями (ВАШ = 0). Для измерений, которые не были выполнены по иным причинам, нежели сон больных, значения ВАШ были получены на пересечении прямой линии, соединяющей данные, измеренные до и после отсутствующих цифр, с требуемой отметкой времени. Если пациенты не сообщали следующие после пропущенных значения ВАШ или выбывали из исследования раньше намеченного срока из-за развития побочных эффектов, последнее доступное значение ВАШ переносилось на все оцениваемые точки времени до конца исследования. Никакие поправки не делались в отношении значений ВАШ в том случае, если пациенты получали резервные обезболивающие средства.
Вторичными переменными эффективности были: максимальная РИБ (РИБmax) в течение первых 8 ч лечения, выраженная как процент по отношению к исходной боли; время, прошедшее до достижения РИБmax; среднее значение РИБ, измеренных спустя 8 ч после начала каждой инфузии (т.е. арифметическое среднее РИБ, рассчитанных для Т8, Т16, Т24, Т32, Т40 и Т48); время, прошедшее до приема резервных обезболивающих средств; количество пациентов, получивших резервные обезболивающие средства в течение всего периода исследования.
Статистический анализ
В основу расчета размера групп была положена первичная конечная точка исследования (первичная переменная эффективности). Расчет был нацелен на то, чтобы добиться 80% мощности при выявлении эквивалентности по этой конечной точке между декскетопрофена трометамолом и кетопрофеном. Граница на уровне 20 % от ожидаемой величины СРИБВ в группе с кетопрофеном служила индикатором эквивалентности двух препаратов.
Первичная переменная эффективности СРИБВ0–8 ч была проанализирована с помощью дисперсионного анализа (ANOVA) с поправками на клинические центры исследования и группы терапии. Влияние отдельных центров на результаты исследования оценивали при уровне значимости 10 %. Были рассчитаны скорректированные групповые средние, стандартные ошибки (СО) и 95% доверительные интервалы (ДИ) для разницы средних между двумя группами терапии. Анальгетическую эффективность двух тестируемых видов лечения считали эквивалентной в том случае, если двусторонний 95% ДИ для разницы между скорректированными средними в каждой из групп терапии полностью вмещался внутри интервала [–T, +T], где Т — это порог, заданный как 20 % от скорректированного среднего значения СРИБВ для группы с кетопрофеном. Вторичные переменные эффективности, так же как и данные о безопасности терапии, анализировали с помощью описательной статистики.
Анализ эффективности выполняли в стартовой и протокольной популяциях. К стартовой популяции относили всех рандомизированных пациентов, которые получили тестируемый препарат и у которых оценивали исходное значение интенсивности боли и по крайней мере одно значение интенсивности боли после приема препарата. Выполнение анализа в протокольной популяции настоятельно рекомендуется в руководствах Международной конференции по гармонизации [17]. К протокольной популяции относили пациентов, которые получили тестируемый препарат, выполнили не менее 50 % оценок интенсивности боли в течение первых 8 ч исследования и не нарушали других основных требований протокола в течение этого периода времени. Все пациенты, получившие по крайней мере одну дозу тестируемого препарата, были включены в анализ безопасности данных средств.
Результаты
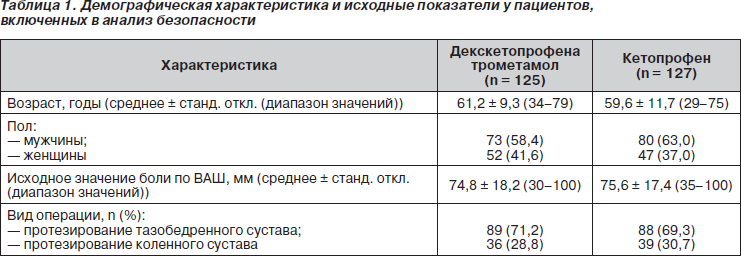
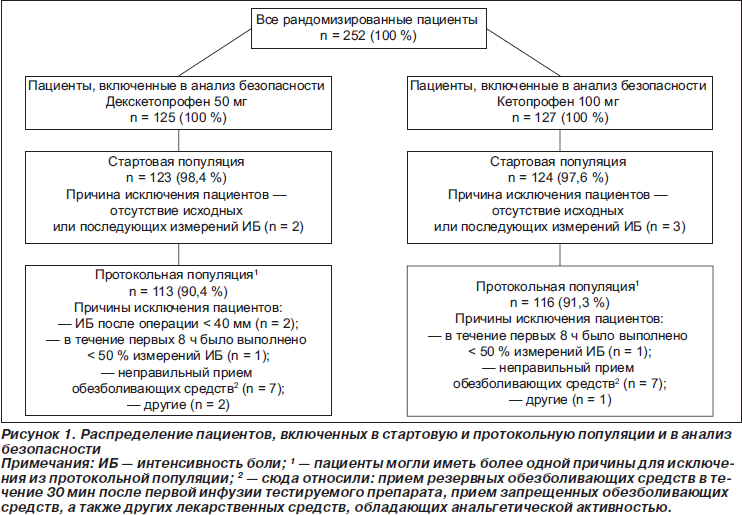
В общей сложности 252 пациента, соответствующих критериям включения в исследование, прошли процедуру рандомизации и были включены в анализ безопасности терапии. Из них 247 пациентов составили стартовую популяцию, 229 — протокольную. Распределение пациентов по популяциям и причины исключения их из той или иной популяции представлены на рис. 1. Из 252 пациентов 153 (60,7 %) были мужчинами. Среднее значение ± станд. откл. возраста пациентов составило 60,4 ± 10,6 года (диапазон значений 29–79 лет). Большинство пациентов были белыми (89 %) и перенесли операцию по поводу протезирования тазобедренного сустава (70 %). Среднее значение ВАШ в исходных условиях составило 75,2 ± 17,0 мм (медиана 77,5). Среди пациентов, включенных в анализ безопасности, не было обнаружено межгрупповых различий в отношении демографической характеристики, вида операции и исходной интенсивности боли, оцененной с помощью ВАШ (табл. 1). В стартовой и протокольной популяции обе группы пациентов также были сравнимы по демографическим характеристикам и исходным показателям (данные не представлены). Что касается комплайенса к лечению, то в общей сложности 117 (93,6 %) пациентов в группе с декскетопрофена трометамолом и 121 (95,3 %) пациент в группе с кетопрофеном получили по шесть инфузий тестируемого препарата. Если говорить о приеме сопутствующей терапии, то 94,4 % пациентов получило низкомолекулярный гепарин (НМГ) для профилактики тромбоза глубоких вен. При этом были использованы различные НМГ в дозах, рекомендуемых для профилактики тромбоза глубоких вен.
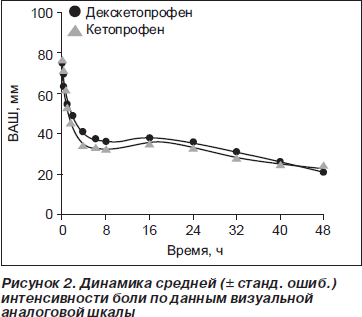
Было показано, что в протокольной популяции оба вида терапии были эквивалентны в плане обезболивающей эффективности, о чем свидетельствуют соответствующие значения первичной переменной эффективности СРИБВ0–8 ч (табл. 2). Влияние отдельных центров на результаты исследований не было значимым. Что касается интенсивности боли, то динамика ее средних значений была одинаковой в обеих группах терапии. При оценке интенсивности боли было выявлено значительное ее ослабление в первые 8 ч в обеих группах терапии, и она продолжала быть ослабленной в течение всего периода исследования (вплоть до 48 ч) (рис. 2). Результаты, полученные в стартовой популяции, были аналогичными (табл. 2).
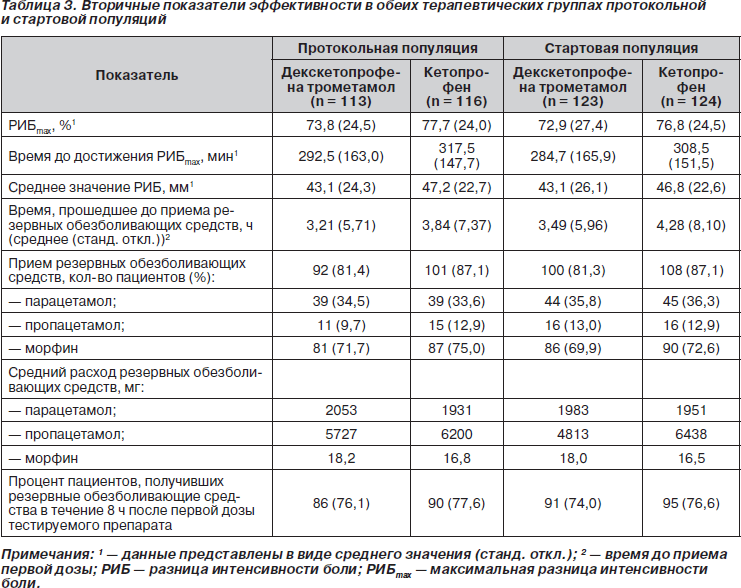
Что касается других параметров, используемых для оценки обезболивающей эффективности (РИБmax, среднее значение РИБ), то не было обнаружено каких-либо различий между двумя видами терапии ни в одной из проанализированных популяций. При этом, однако, время, прошедшее до достижения РИБmax, было несколько короче в группе с декскетопрофена трометамолом, а процент пациентов, которым были назначены резервные обезболивающие средства, был несколько выше в группе с кетопрофеном (табл. 3).
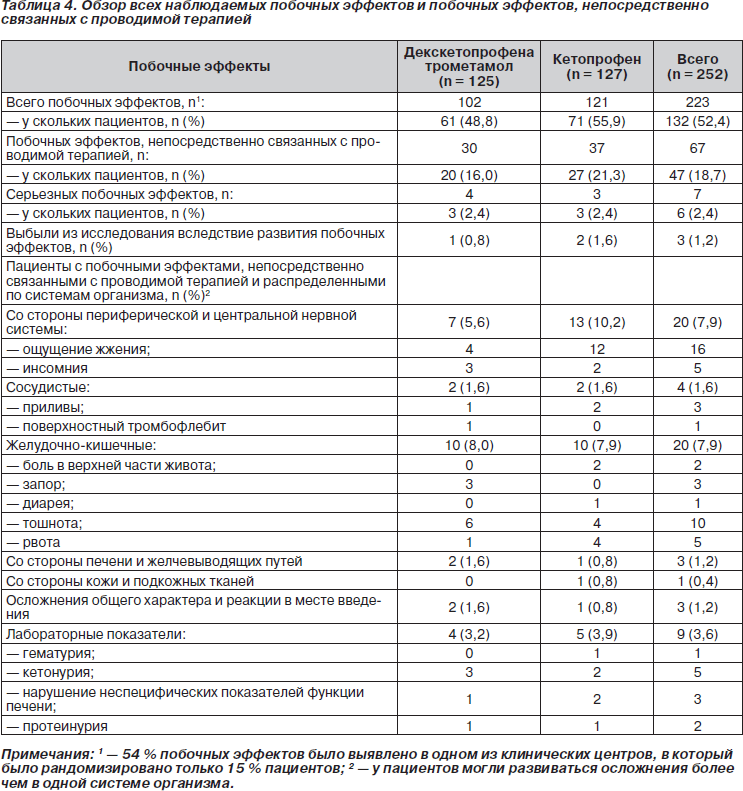
В общей сложности 132 (52,4 %) пациента сообщили о развитии 223 побочных эффектов (табл. 4). Доля пациентов с побочными эффектами была ниже в группе с декскетопрофена трометамолом (48,8 %) по сравнению с группой, получавшей кетопрофен (55,9 %). Необходимо отметить, что только у 47 (18,7 %) пациентов наблюдались побочные эффекты, непосредственно связанные с проводимой терапией. В ходе исследования не умер ни один из пациентов, но было зарегистрировано семь серьезных побочных эффектов у шести пациентов (по три в каждой группе). В группе с декскетопрофена трометамолом наблюдались тромбоз, эмфизема кожи и остановка сердца, за которой следовал эпизод тромбоэмболии легочной артерии (каждый из перечисленных побочных эффектов наблюдался однократно), однако ни одно из этих осложнений не было расценено как связанное с проводимым лечением. В группе с кетопрофеном наблюдались тромбоз глубокой вены конечности, дислокация сустава и поверхностная раневая инфекция (каждый из перечисленных побочных эффектов наблюдался однократно); эти осложнения также не были расценены как связанные с проводимым лечением.
Из нашего исследования вследствие развития побочных эффектов выбыло в общей сложности три пациента (два в группе с кетопрофеном), однако ни один из этих побочных эффектов не был классифицирован как серьезный. В группе с кетопрофеном причинами выбывания пациентов из исследования стали случаи гиповолемии и психотического синдрома, в то время как в группе с декскетопрофена трометамолом пациент выбыл вследствие тремора. Два перечисленных побочных эффекта в группе с кетопрофеном расценили как не связанные с проводимой терапией, а побочный эффект в группе с декскетопрофена трометамолом — как возможно связанный с приемом препарата.
Доля пациентов с побочными эффектами, связанными с проводимой терапией, была ниже в группе с декскетопрофена трометамолом (16 %) по сравнению с группой с кетопрофеном (21,3 %). Наиболее часто регистрируемыми побочными эффектами, связанными с проводимой терапией, были ощущение жжения в месте инъекции — 16 (6,3 %) пациентов (4 (3,2 %) чел. в группе с декскетопрофена трометамолом и 12 (9,4 %) — с кетопрофеном), тошнота — 10 (4,0 %) пациентов (6 (4,8 %) чел. в группе с декскетопрофена трометамолом и 4 (3,1 %) — с кетопрофеном), а также инсомния, рвота и кетонурия — каждое из этих трех осложнений наблюдалось у пяти пациентов. Примечательно, что в ходе исследования не было зафиксировано случаев послеоперационного кровотечения. Не наблюдалось изменений артериального давления и частоты сердечных сокращений. Побочных эффектов со стороны мочевыводящей системы и нарушений лабораторных показателей, отражающих функцию почек (уровень креатинина), обнаружено не было. Клинически значимые лабораторные нарушения в конце лечения наблюдались у очень ограниченного числа пациентов по сравнению с наличием таких нарушений в исходных условиях; достоверных различий между группами не наблюдалось (табл. 4).
Обсуждение
Настоящее многоцентровое рандомизированное двойное слепое параллельно-групповое клиническое исследование фазы III было выполнено для того, чтобы оценить обезболивающую эффективность новой лекарственной формы декскетопрофена трометамола, представляющей собой раствор для внутривенного введения, по сравнению с кетопрофеном у пациентов с умеренной и тяжелой послеоперационной болью после протезирования тазобедренного или коленного сустава (т.е. по своему характеру наше исследование было исследованием эквивалентности). Ранее было показано, что внутривенное введение кетопрофена было более эффективным по сравнению с плацебо в обеспечении анальгезии и снижении требуемой дозы резервных обезболивающих средств у пациентов, которым выполняют протезирование тазобедренного или коленного сустава [16]. Это позволило нам выполнить настоящее исследование как исследование эквивалентности декскетопрофена трометамола и кетопрофена (без включения плацебо-группы).
НПВС уже достаточно длительное время применяют в качестве обезболивающих средств, и в ряде исследований было показано, что после оперативных вмешательств они обеспечивают ослабление боли, эквивалентное таковому опиоидов или даже лучшее [18–22]. После средних и больших операций рекомендуют применять НПВС в комбинации с опиоидами в рамках сбалансированного подхода к анальгезии или мультимодального подхода к лечению послеоперационной боли [23–25]. Преимущества подобного подхода сводятся к достижению достаточной анальгезии в результате аддитивного или синергического эффектов между различными обезболивающими средствами, вместе со снижением количества побочных эффектов вследствие снижения доз каждого из используемых обезболивающих средств и различий в профиле побочных эффектов каждого из применяемых препаратов. Однако цель настоящего исследования сводилась к определению анальгетической эффективности двух НПВС на основе оценки интенсивности боли; морфин и другие обезболивающие средства использовались в качестве резервных средств и не применялись на регулярной основе.
В ходе настоящего исследования процедуре рандомизации подверглось в общей сложности 252 пациента, большинство из которых было белыми, мужчин было больше, чем женщин. Чаще выполнялось протезирование тазобедренного сустава, чем коленных суставов. Между пациентами двух выделенных групп лечения не было достоверных различий по демографической характеристике и исходным показателям. Основной анализ был выполнен у 229 пациентов, входивших в состав протокольной популяции. Необходимо отметить, что в ходе нашего исследования высокий процент пациентов получил резервные обезболивающие средства, главным образом морфин (> 75 % пациентов в течение первых 8 ч). Однако этот результат был вполне ожидаем, если учесть характер операций, которые переносили больные, и высокий средний исходный уровень боли, достигающий 75 мм по ВАШ. Эти данные согласуются с лечебными рекомендациями по комбинированию различных обезболивающих средств после средних по объему операций в рамках сбалансированного подхода к обезболиванию. С другой стороны, отсутствие плацебо-группы, т.е. пациентов, получавших только резервные обезболивающие средства, ограничивает интерпретацию полученных результатов в плане получения истинной величины обезболивающего эффекта у каждого из двух протестированных НПВС. Тем не менее сравнимость исходных характеристик между группами и высокий исходный уровень боли подтверждает, по крайней мере отчасти, адекватную чувствительность использованной нами модели боли.
Согласуясь с результатами предыдущих исследований, оценивающих применение декскетопрофена трометамола перорально или внутримышечно при различных клинических ситуациях [7, 10–12, 25, 26], результаты настоящего исследования свидетельствуют о том, что после внутривенного введения декскетопрофена трометамол так же эффективен и хорошо переносится, как и кетопрофен при лечении послеоперационной боли после крупных ортопедических операций. Эти два препарата были эквивалентны в отношении обезболивающей эффективности, что следует из соответствующих значений выбранной первичной переменной эффективности (СРИБВ0–8 ч). Более того, динамика обезболивающего эффекта обоих препаратов в значительной степени накладывалась одна на другую в течение всего периода оценивания боли. Также не было обнаружено различий в отношении таких вторичных переменных эффективности, как РИБmax и среднее значение РИБ. Период времени, прошедший до достижения РИБmax, будучи непрямой мерой начала обезболивающего эффекта, был короче для группы с декскетопрофена трометамолом, хотя достоверных различий получено не было.
Что касается профиля безопасности, то результаты были сопоставимы с теми, которые были получены в предыдущих исследованиях. И хотя данные о безопасности были получены главным образом в кратковременных испытаниях [9–11, 13, 14], у пациентов с остеоартрозом коленного сустава обнаружена тенденция к лучшей переносимости декскетопрофена по сравнению с кетопрофеном спустя 3 недели терапии [12]. Более того, в недавно опубликованных результатах многоцентрового исследования, выполненного по типу «случай — контроль», сообщалось, что риск развития кровотечения из верхних отделов желудочно-кишечного тракта при применении декскетопрофена был ниже по сравнению с таковым кетопрофена [27]. В ходе настоящего исследования оба препарата хорошо переносились, хотя в группе с декскетопрофена трометамолом наблюдалось меньшее число пациентов с побочными эффектами, как не связанными, так и непосредственно связанными с проводимой терапией. Ни один из серьезных побочных эффектов, развившихся в ходе настоящего исследования, не был связан с приемом тестируемых препаратов. Ощущение жжения, возникающее в месте инъекции, было наиболее частым побочным эффектом, за которым следовали тошнота, рвота, инсомния и кетонурия. Однако из 16 случаев ощущения жжения в месте инъекции, связанного с вводимым препаратом, большая часть наблюдалась в группе с кетопрофеном (12 случаев). Каких-либо нарушений лабораторных показателей, отражающих функцию почек, в ходе исследования обнаружено не было.
Оценка профиля безопасности тестируемых препаратов отчасти была сфокусирована на потенциальном взаимодействии с НМГ, введение которых является частью стандартных терапевтических процедур для предотвращения тромбоза глубоких вен у пациентов, подвергающихся ортопедическим операциям. Большая часть пациентов, включенных в настоящее исследование, получала сопутствующую терапию НМГ, но каких-либо случаев послеоперационного кровотечения обнаружено не было.
Выводы
Результаты настоящего исследования подтверждают терапевтическую эквивалентность обезболивающей эффективности энантиомерически эквивалентных доз декскетопрофена трометамола и кетопрофена, вводимых внутривенно, при лечении послеоперационной боли после протезирования тазобедренного или коленного сустава. Высокий процент пациентов, которым потребовалось назначение резервных обезболивающих средств, указывает на необходимость применения мультимодального подхода к устранению боли после данного типа операций. В ходе исследования была обнаружена тенденция к лучшей переносимости декскетопрофена трометамола по сравнению с кетопрофеном, однако подтвердить эти данные может только интенсивное применение препарата в реальной клинической практике и результаты качественно выполненных обсервационных исследований.
Результаты настоящего исследования были отчасти представлены на 10-м Всемирном конгрессе IASP (Международная ассоциация по изучению боли), посвященном боли, который состоялся 17–22 августа 2002 г. в Сан-Диего (Калифорния, США). Исследование было выполнено при финансовой поддержке Menarini Ricerche SpA (Флоренция, Италия).
Перевод А.В. Савустьяненко
Оригинал статьи опубликован в Clin. Drug Invest. 2006; 26(9): 517-528
Ferreira S.H., Vane J.R. New aspects of the mode of action of non-steroidal anti-inflammatory drugs // Ann. Rev. Pharmacol. — 1974. — 14. — 57-73.
Cashman J.N. The mechanism of action of NSAIDs in analgesia // Drugs. — 1996. — 52, Suppl. 5. — 13-23.
Veys E.M. 20 year’s experience with ketoprofen // Scand. J. Rheumatol. — 1991. — 90, Suppl. — 1-44.
Sunshine A., Olson N.Z. Analgesic efficacy of ketoprofen in postpartum, general surgery and chronic cancer pain // J. Clin. Pharmacol. — 1988. — 28 (12 Suppl.). — 47-54.
Mauleon D., Artigas R., Garcia M.L. et al. Preclinical and clinical development of dexketoprofen trometamol // Drugs. — 1996. — 52, Suppl. 5. — 24-46.
Caldwell J., Hutt A.J., Fournel-Gigleux S. The metabolic chiral inversion and dispositional enantioselectivity of the 2-arylpropionic acids and their biological consequences // Biochem. Pharmacol. — 1988. — 37. — 105-14.
Barbanoj M.J., Gich I., Artigas R. et al. Pharmacokinetics of dexketoprofen trometamol in healthy volunteers after single and repeated doses // J. Clin. Pharmacol. — 1998. — 38 (12 Suppl.). — 33S-40S.
Marenco J.L., Perez M., Navarro F.J. et al. A multicentre, randomised, double-blind study to compare the efficacy and tolerability of dexketoprofen trometamol versus diclofenac in the symptomatic treatment of knee osteoarthritis // Clin. Drug Invest. — 2000. — 19. — 247-56.
Rodriguez M.J., Contreras D., Galvez R. et al. Double-blind evaluation of short-term analgesic efficacy of orally administered dexketoprofen trometamol and ketorolac in bone cancer pain // Pain. — 2003. — 104. — 103-10.
McGurk M., Robinson P., Rajayogeswaran V. et al. Clinical comparison of dexketoprofen trometamol, ketoprofen, and placebo on dental pain // J. Clin. Pharmacol. — 1998. — 38 (12 Suppl.). — 46S-54S.
Ezcurdia M., Cortejoso F.J., Lanzon R. et al. Comparison of the efficacy and tolerability of dexketoprofen and ketoprofen in the treatment of primary dysmenorrhea // J. Clin. Pharmacol. — 1998. — 38 (12 Suppl.). — 65S-73S.
Beltran J., Martin-Mola E., Figueroa M. et al. Comparison of dexketoprofen trometamol and ketoprofen in the treatment of osteoarthritis of the knee // J. Clin. Pharmacol. — 1998. — 38 (12 Suppl.). — 74S-80S.
Hanna M.H., Elliot K.M., Stuart-Taylor M.E. et al. Comparative study of analgesic efficacy and morphine-sparing effect of intramuscular dexketoprofen trometamol with ketoprofen or placebo after major orthopaedic surgery // Br. J. Clin. Pharmacol. — 2003. — 55. — 126-33.
Sanchez-Carpena J., Sesma-Sanchez J., Sanchez-Juan C. et al. Comparison of dexketoprofen trometamol and dipyrone in the treatment of renal colic // Clin. Drug Invest. — 2003. — 23. — 139-52.
Kehlet H., Dahl J.B. Anaesthesia, surgery, and challenges in postoperative recovery // Lancet. — 2003. — 362. — 1921-8.
Kostamovaara P.A., Laitinen J.O., Nuutinen L.S. et al. Intravenous ketoprofen for pain relief after total hip or knee replacement // Acta Anaesthesiol. Scand. — 1996. — 40. — 697-703.
European Medicines Agency. ICH Topic E9. Note for guidance on statistical principles for clinical trials (CPMP/ICH/363/96). London, 1998 September.
McLoughlin C., McKinney M.S., Fee J.H.P. et al. Diclofenac for day-care arthroscopy surgery: comparison with standard opioid therapy // Br. J. Anaesth. — 1993. — 65. — 620-3.
Gilles G.W.A., Kenny G.N.C., Bulligham R.E.S. et al. The morphine sparing effect of ketorolac promethamine // Anaesthesia. — 1987. — 42. — 727-31.
Reasbeck P.G., Rice M.L., Reasbeck J.C. Double-blind controlled trial of indomethacin as an adjunct to narcotic analgesia after major abdominal surgery // Lancet. — 1982. — 2. — 115-8.
Lindgren U., Djupsjo H. Diclofenac for pain after hip surgery // Acta Orthop. Scand. — 1985. — 56. — 28-31.
Moote C. Efficacy of nonsteroidal anti-inflammatory drugs in the management of postoperative pain // Drugs. — 1992. — 44, Suppl. 5. — 14-30.
Code W. NSAIDs and balanced analgesia // Can. J. Anesth. — 1993. — 40. — 401-5.
Rorarius M.G.F., Baer G.A. Non-steroidal anti-inflammatory drugs for postoperative pain relief // Curr. Opin. Anaesthesiol. — 1994. — 7. — 358-62.
EuroPain Task Force. European minimum standards for the management of postoperative pain. — Goring-on-Thames, UK: Pegasus Healthcare International, 1998.
Bagan J.V., Lopez Arranz J.S., Valencia E. et al. Clinical comparison of dexketoprofen trometamol and dipyrone in postoperative dental pain // J. Clin. Pharmacol. — 1998. — 38 (12 Suppl.). — 55S-64S.
Laporte J.L., Ibanez L., Vidal X. et al. Upper gastrintestinal bleeding associated with the use of NSAIDs: newer versus older agents // Drug Saf. — 2004. — 27(6). — 411-20.