Международный неврологический журнал Том 21, №6, 2025
Вернуться к номеру
Хронічний біль у психіатричному вимірі: клініко-психопатологічні маркери ризику оперантної поведінки за даними шкали DIRE
Авторы: A.E. Asanova (1), О.О. Khaustova (1), R.A. Abdriakhimov (2)
(1) - Bogomolets National Medical University, Kyiv, Ukraine
(2) - Academy of Labour, Social Relations, and Tourism, Kyiv, Ukraine
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
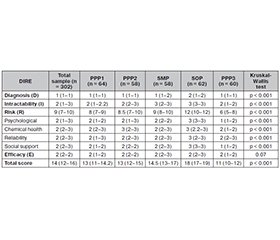
Актуальність. Хронічний біль — це складний біопсихосоціальний феномен, що поєднує соматичні, психоемоційні та соціальні компоненти. Одним із ключових ускладнень хронічного болю є формування оперантної (дисфункціональної) поведінки, яка підвищує ризик неефективності терапії та залежності від опіоїдної аналгезії. Матеріали та методи. У програму дослідження були включені 302 амбулаторнi пацієнти віком від 18 до 70 років із діагнозом хронічного болю, що тривав більше трьох місяців. Проаналізовано соціально-демографічні, клінічні та клініко-психопатологічні характеристики учасників із хронічними больовими розладами й синдромами. Усі пацієнти були розподілені на наступні групи: первинно-психічний біль (ППБ1), психофізіологічний біль (ПФБ2), змішаний первинно-психічний та психофізіологічний біль (ППБ3), вторинний змішаний біль (ВЗБ), вторинний органічний біль (ВОБ). Проведено обстеження за шкалою DIRE. Результати. Виявлені відмінності між групами, очевидно, асоційовані з патогенезом захворювання, а не соціально-демографічними характеристиками хворих. Пацієнти групи ППБ3 мають найбільші ризики формування оперантної поведінки та залежності від опіоїдних препаратів, особи з групи ВОБ — найменші або такі, що можна розглядати як малоймовірні. Результати в групах ППБ1, ПФБ2 і ВЗБ вказують на те, що ППБ1 і ПФБ2 не відрізняються і мають проміжні ризики, а ВЗБ гіпотетично може мати нижчі. Висновки. Перехід ВОБ у ВЗБ — це не фізіологічна еволюція болю, а наслідок невчасно розпізнаних психосоціальних чинників. Його профілактика можлива лише за умов інтегрованого ведення пацієнта, коли лікар одночасно керує соматичним процесом і модулює психоемоційну відповідь. Таким чином, найкращою профілактикою переходу ВОБ в ВЗБ є рання проактивна психоемоційна корекція, когнітивно-поведінкове навчання й соціальна активізація, що реалізуються в межах мультимодальної персоналізованої курації хронічного болю.
Background. Chronic pain is a complex biopsychosocial phenomenon that integrates somatic, psycho-emotional, and social dimensions. One of its key complications is the development of operant (dysfunctional) pain behavior, which increases the risk of therapeutic inefficacy and dependence on opioid analgesia. Materials and methods. The study included 302 outpatients aged 18–70 years diagnosed with chronic pain lasting more than 3 months. Sociodemographic, clinical, and clinico-psychopathological characteristics of patients with chronic pain disorders and syndromes were analyzed. All participants were divided into 5 groups: primary psychogenic pain (PPР1); psychophysiological pain (PPP2); mixed primary psychogenic and psychophysiological pain (PPP3); secondary mixed pain (SMP); secondary organic pain (SOP). All patients were assessed using the DIRE scale to determine suitability for opioid therapy and behavioral risk. Results. Significant differences between groups were observed, primarily associated with the pathogenesis of pain, rather than sociodemographic characteristics. Patients in group PPP3 demonstrated the highest risk of operant behavior and opioid dependence, while those in group SOP had the lowest risk. The findings in groups PPP1, PPP2, and SMP indicate that PPP1 and PPP2 did not differ significantly and showed intermediate risk levels, whereas SMP was associated with slightly lower risks. Conclusions. The transition from secondary organic pain to secondary mixed pain should not be considered a physiological evolution of pain but rather a consequence of unrecognized psychosocial factors. Prevention of such transition is possible only through integrated patient management in which the clinician simultaneously addresses the somatic process and modulates the psycho-emotional response.
оперантна поведінка; дисфункціональна больова поведінка; хронічний біль; опіоїдна терапія; психосоціальні фактори; шкала DIRE
operant behavior; dysfunctional pain behavior; chronic pain; opioid therapy; psychosocial factors; DIRE scale