На сьогодні фібриляція передсердь (ФП) є однією з найпоширеніших аритмій у клінічній практиці. За даними епідеміологічних досліджень, щорічно число хворих, які страждають на це порушення серцевого ритму, неухильно збільшується, а поширеність у загальній популяції становить понад 2 % [1]. Незважаючи на те, що ФП не є життєзагрозливою аритмією, вона призводить до підвищення ризику тромбоемболічних ускладнень, зокрема ішемічного інсульту, зменшення очікуваної тривалості життя та погіршення якості життя пацієнтів. Саме тому соціальна значимість цього порушення серцевого ритму надзвичайно висока.
Зі збільшенням віку поширеність ФП неухильно зростає, найбільш високі показники захворюваності на ФП виявляються у пацієнтів старше від 80 років. У більшості великих епідеміологічних досліджень показано, що виявлення різних форм ФП становить не більше ніж 1 % серед пацієнтів молодше від 60 років і досягає 6 % у старшій віковій групі [2].
ФП робить великий негативний внесок у розвиток закономірних змін серцево-судинної системи. Вперше у Фрамінгемському дослідженні показано, що тривале персистування ФП сприяє розвитку і прогресуванню серцевої недостатності, ремоделюванню камер серця, підвищує ризик смерті від серцево-судинних ускладнень у пацієнтів з артеріальною гіпертензією, ішемічною хворобою серця, некоронарогенними захворюваннями міокарда [3].
Рекомендації Європейського товариства кардіологів з діагностики та лікування ФП — 2024: принцип AF-CARE
В основу стратегії ведення пацієнтів з фібриляцією передсердь в рекомендаціях Європейського товариства кардіологів з діагностики та лікування ФП 2024 року покладений принцип AF-CARE (рис. 1).
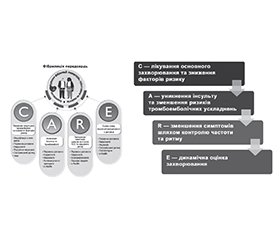
Терапія CARE, згідно з рекомендаціями ESC 2024, передбачає такі кроки (рис. 2).
Фармакологічний контроль ЧСС у світі рекомендацій ESC-2024
Згідно з рекомендаціями ESC-2024, фармакологічний контроль частоти серцевих скорочень (ЧСС) може бути досягнутий бета-блокаторами, дигоксином, дилтіаземом і верапамілом або комбінованою терапією. Деякі антиаритмічні препарати (аміодарон, дронедарон, соталол) також знижують ЧСС, проте вони повинні використовуватися тільки у пацієнтів, які потребують контролю ритму серця. Вибір терапії, що знижує ЧСС, залежить від симптомів, наявності супутньої патології і потенційних побічних ефектів [4].
Бета-блокатори часто застосовуються як терапія першої лінії для контролю ЧСС через сприятливий профіль ефективності та безпеки. Недигідропіридинові блокатори кальцієвих каналів (НДБКК) — верапаміл і дилтіазем забезпечують прийнятний контроль ЧСС та поліпшують симптоми у пацієнтів з ФП. В одному невеликому дослідженні у пацієнтів зі збереженою фракцією викиду лівого шлуночка НДБКК не погіршували толерантність до фізичного навантаження і приводили до зниження натрійуретичного пептиду типу В.
Дигоксин і дигітоксин неефективні у пацієнтів з надмірною активацією симпатичної нервової системи. У спостережних дослідженнях прийом дигоксину був асоційований з підвищеною смертністю пацієнтів з ФП. У свою чергу, низькі дози дигоксину можуть бути асоційовані зі сприятливим прогнозом.
Аміодарон з метою зменшення ЧСС може бути призначений у виняткових випадках, коли не вдається контролювати ЧСС за допомогою комбінованої терапії у пацієнтів, у яких не може бути розглянутий нефармакологічний контроль частоти (абляція атріовентрикулярного (АВ) вузла і постійна електрокардіостимуляція), незважаючи на несприятливі позасерцеві побічні ефекти препарату [4].
Антиаритмічні засоби для відновлення синусового ритму, рекомендовані ЕSC-2024
Стратегія контролю ритму спрямована на відновлення і підтримку синусового ритму (СР) і включає комбінацію лікувальних підходів: кардіоверсію, призначення антиаритмічних препаратів і катетерну абляцію [4].
Фармакологічна кардіоверсія є плановою процедурою і показана пацієнтам зі стабільною гемодинамікою. Її справжня ефективність оцінюється за спонтанним відновленням синусового ритму протягом 48 год від моменту госпіталізації у 76–83 % пацієнтів з недавнім пароксизмом ФП (10–18 % — протягом перших 3 год, 55–66 % — протягом 24 год, 69 % — протягом 48 год). Тому вичікувальна тактика (зазвичай < 24 год) може розглядатися у пацієнтів з недавнім пароксизмом ФП як альтернатива ранньої кардіоверсії.
Для відновлення синусового ритму ESC-2024, залежно від типу і тяжкості супутнього захворювання серцево-судинної системи, рекомендує вибір наступних ААП: флекаїнід, пропафенон, аміодарон, ібутилід або вернакалант. В Україні для фармакологічної кардіоверсії препаратами вибору є флекаїнід (пероральний), пропафенон та аміодарон.
Флекаїнід має рекомендацію найвищого класу 1A для фармакологічної конверсії ритму при епізодах ФП. Початкова доза флекаїніду становить 200–300 мг або 1–2 мг/кг протягом 10 хвилин для пероральної та внутрішньовенної форми відповідно; при довгостроковій терапії — 50–150 мг двічі на день. Частка успіху для перорального флекаїніду становить 50–60 % через 3 години, 75–80 % через 3–8 годин; внутрішньовенного флекаїніду — 52–95 % протягом 6 годин [4, 11].
Пропафенон призначається перорально 450–600 мг або внутрішньовенно 1,5–2 мг/кг протягом 10 хвилин; довгостроково — 150–300 мг тричі на день. При використанні пропафенону 45–55 % пацієнтів достигають успіху лікування через 3 години, 69–78 % — через 8 годин.
Протипоказаннями для призначення флекаїніду та пропафенону є виражені структурні зміни міокарда (за умови наявності активної ішемії), синдром Бругада або виражена хронічна хвороба нирок (КК < 35 мл/хв). Перед використанням «таблеток у кишені» рекомендується отримати попередню інформацію щодо їх безпеки та ефективності в стаціонарних умовах. Для профілактики розвитку тріпотіння передсердь з проведенням 1 : 1 або 2 : 1 слід призначати бета-блокатори за умови відсутності протипоказань (брадикардія, АВ-блокади). Також слід дотримуватися обережності пацієнтам із захворюванням синусового вузла та дисфункцією AVN (головним чином для пропафенону) та не використовувати ці препарати для конверсії СР при тріпотінні передсердь [4].
/9.jpg)
Аміодарон призначається внутрішньовенно — 300 мг в/в протягом 30–60 хвилин, при довгостроковому підході — 900–1200 мг в/в протягом 24 годин (або перорально 200 мг 3 рази на день протягом 4 тижнів). Частка успішної терапії становить 44 % через 8–12 годин до кількох днів. Побічними ефектами призначення аміодарону може бути флебіт, гіпотензія, брадикардія/атріовентрикулярна блокада, подовження інтервалу QT, тиреотоксикоз.
Аміодарон рекомендований пацієнтам із ФП та СН зі зниженою ФВ, які потребують тривалої антиаритмічної терапії для запобігання рецидиву та прогресуванню ФП, з ретельним розглядом та моніторингом екстракардіальної токсичності (клас ІА). Дронедарон — пацієнтам із ФП, які потребують тривалого контролю ритму, включно з СН з помірно зниженою ФВ та СН зі збереженою ФВ (клас ІА). Флекаїнід або пропафенон рекомендовані пацієнтам з ФП, які потребують тривалого контролю ритму для запобігання рецидиву та прогресуванню ФП, за винятком пацієнтів із порушеннями систолічної функції лівого шлуночка, тяжкою гіпертрофією лівого шлуночка або ішемічною хворобою серця (клас ІА). Щоб запобігти провідності 1 : 1, яка трансформується в тріпотіння передсердь, слід розглянути можливість одночасного застосування бета-блокаторів, дилтіазему або верапамілу у пацієнтів з ФП, які отримують флекаїнід або пропафенон (клас ІС). Соталол можна розглянути у пацієнтів із ФП, яким потрібен тривалий контроль ритму з нормальною ФВ ЛШ або ішемічною хворобою серця, щоб запобігти рецидиву та прогресуванню ФП, але його використання вимагає ретельного моніторингу інтервалу QT, рівня калію в сироватці крові, функції нирок та інших факторів ризику (ІІвА). Антиаритмічна терапія не рекомендована пацієнтам із прогресуючими порушеннями провідності, якщо не передбачена антибрадикардійна стимуляція (ІІІС) [4].
Антиартимічна ефективність флекаїніду при ФП
У багатьох клінічних дослідженнях вивчалась ефективність флекаїніду для конверсії ритму при ФП. Фармакокінетика флекаїніду при пероральному прийомі характеризується високою біодоступністю (90–95 %) і відсутністю ефекту первинної метаболізації в печінці. Пікова концентрація препарату в крові досягається впродовж 1–4 год, у цей період можна очікувати його максимальну дію та конверсію ритму [5, 6].
У п’ятьох рандомізованих контрольованих дослідженнях із групами активного контролю флекаїнід виявив перевагу над іншим ААП ІС класу, що застосовують при ФП, — пропафеноном. Ефективність конверсії ритму в групах флекаїніду була вищою і становила від 50 до 90 % як при в/в застосуванні, так і при використанні стратегії «таблетка в кишені», тоді як пропафенону — від 25 до 72 % (рис. 3) [7].
При порівнянні флекаїніду з аміодароном було виявлено, що коефіцієнт конверсії ФП протягом 3 годин вищий при застосуванні перорального флекаїніду — 66 % порівняно з внутрішньовенним аміодароном — 25 %. У момент часу 8-годинний коефіцієнт конверсії ФП був вищий при внутрішньовенному введенні флекаїніду порівняно з внутрішньовенним аміодароном — 73 проти 53 % (рис. 4) [7].
У метааналізі рандомізованих випробувань оцінювалася ефективність різних ААП (аміодарону, дофетиліду, флекаїніду, ібутиліду, прокаїнаміду, вернакаланту) для конверсії ФП. Була виявлена стабільна перевага флекаїніду над іншими ААП в лікуванні пароксизму ФП. Також показано, що протягом 4 годин 56 % (5 із 10) пацієнтів досягнуть СР при застосуванні флекаїніду, тоді як при застосуванні пропафенону — 45 % (4 із 10); протягом доби — 81 % (8 із 10) пацієнтів та 45 % (4 із 10) відповідно [8].
Не проводилося досліджень прямого порівняння флекаїніду з дофетилідом і вернакалантом, але за даними випробувань із плацебо-контролем ефективність обох препаратів була нижчою, ніж флекаїніду [8]. Таким чином, наявна доказова база дозволяє з упевненістю вважати флекаїнід найефективнішим серед усіх класів ААП для конверсії ритму при ФП у пацієнтів без структурної патології серця.
Тривале застосування ААП для підтримки СР при ФП
Підтримка синусового ритму є важливою клінічною метою при ФП, оскільки дозволяє знизити смертність та серцево-судинні ускладнення. У багатьох дослідженнях порівнювалася ефективність флекаїніду з іншими ААП.
Рівень підтримки синусового ритму серед користувачів флекаїніду/пропафенону при 6-місячному спостереженні оцінювався у дослідженні R.M. Sánchez Soriano et al. [10], аллапініну/етацизину/аміодарону при 3-місячному спостереженні — у дослідженні С.Ф. Соколова і співавт. [13]. Було показано зменшення ефективності етацизину від 42 % при тривалому спостереженні 3 місяці до 32 %, а також зафіксовано близько 40 % кардіальних побічних явищ (тріпотіння передсердь, шлуночкових аритмій), достатніх для відміни антиаритмічного препарату. Для аміодарону частка респондерів з утриманням синусового ритму становила 64 %, для флекаїніду — 63 %, для пропафенону — 53 % при 6-місячному спостереженні (рис. 5). Таким чином, флекаїнід гарантує більше шансів на успіх в утриманні СР при ФП.
У проспективному відкритому сліпому дослідженні Flec-SL взяли участь пацієнти з персистуючою ФП, яким проводилася планова кардіоверсія, а після неї — рандомізація в групу лікування флекаїнідом (200–300 мг/день) протягом 4 тижнів (короткий курс лікування), групу лікування флекаїнідом протягом 6 місяців (тривалий курс лікування) або групу контролю [12].
Первинна кінцева точка була комбінованою і включала рецидив персистуючої ФП або смерть. За результатами 4-тижневого спостереження, відсутність досягнення первинної кінцевої точки спостерігалась у 70,2 % пацієнтів групи флекаїніду проти 52,5 % групи конт–ролю (Р = 0,016). Рецидиви ФП виявлялися у 120 (46 %) з 261 пацієнта, який отримував короткий курс, та у 103 (39 %) з 263 пацієнтів, які отримували тривалий курс терапії флекаїнідом. Автори дійшли висновку, що короткий курс терапії флекаїнідом істотно знижує ризик рецидиву ФП, при цьому тривалий курс показує кращі результати терапії.
Порівняння ефективності флекаїніду і дронедарону для підтримки синусового ритму після електрокардіоверсії персистуючої ФП у пацієнтів з мінімальним структурним захворюванням серця або без нього було проведено у метааналізі H. Wilson et al. [14] з включенням 9 досліджень, що охоплювали 1349 пацієнтів зі стійкою формою ФП. У двох ретроспективних дослідженнях продемонстровано зниження рецидиву ФП на 6 % при прийомі флекаїніду порівняно з дронедароном. В одному РКД виявлено зниження ризику рецидиву ФП на 28 % при призначенні дронедарону порівняно з плацебо через 6 місяців лікування. У двох РКД флекаїнід знижував рецидив ФП на 16 % порівняно з плацебо через 6–12 місяців. Протягом періоду спостереження від 6 до 12 місяців вивчалася комбінована частота рецидивів ФП, при якій флекаїнід і дронедарон підтримували СР в 50 і 42 % випадків відповідно (рис. 6).
Таким чином, флекаїнід та дронедарон продемонстрували подібну ефективність у підтримці СР у пацієнтів після електрокардіоверсії з приводу персистуючої ФП. Однак підтримка СР була більш значущою у групі флекаїніду, ніж у групі дронедарону.
Стратегія «таблетка в кишені»
Стратегія застосування флекаїніду «таблетка в кишені» підходить для попередньо обстежених пацієнтів, які здатні ідентифікувати у себе початок епізоду ФП за симптоматикою або сигналами портативного чи імплантованого пристрою з функцією моніторування ЕКГ [4]. Зазвичай терапія першого епізоду ФП проходить в умовах стаціонару, де проводять попередню оцінку її безпеки та ефективності. Після успішного застосування флекаїніду для відновлення СР та за відсутності побічних ефектів таблетований флекаїнід може бути призначений для лікування вдома. Стратегія «таблетка в кишені» означає, що відповідним чином навчений пацієнт може завжди мати ліки при собі й самостійно прий-няти навантажувальну дозу флекаїніду 200 або300 мг одноразово для переривання повторних епізодів ФП. Оскільки хворий швидко приймає препарат після появи аритмії, це забезпечує зменшення звернень у відділення невідкладної допомоги (ВНД), потреби в електрокардіоверсії та госпіталізації.
Ефективність амбулаторного лікування ФП за допомогою стратегії «таблетка в кишені» була вивчена у дослідженні Alboni et al. [9]. Флекаїнід або пропафенон призначали перорально для відновлення синусового ритму у 268 пацієнтів з ФП. Із цих пацієнтів 58 (22 %) були виключені із дослідження через невдачу лікування або побічні ефекти. Інші 210 пацієнтів самостійно прий-
мали флекаїнід або пропафенон (підхід «таблетка в кишені») після початку серцебиття.
Протягом 15 ± 5 місяців у 165 пацієнтів (79 %) було виявлено 618 епізодів аритмії. З цих епізодів 569 (92 %) лікувалися через 36 ± 93 хвилини після появи симптомів. Лікування було успішним у 534 епізодах (94 %); час зникнення симптомів становив 113 ± 84 хвилини. Серед 165 пацієнтів з рецидивами препарат був ефективним протягом усіх епізодів аритмії у 139 пацієнтів (84 %). Побічні ефекти були зареєстровані у 12 пацієнтів (7 %), включно з тріпотінням передсердь у 1 пацієнта і несерцевими побічними ефектами в 11 пацієнтів. Кількість щомісячних відвідувань відділень невідкладної допомоги та госпіталізацій була значно нижчою під час спостереження, ніж за рік до цільового епізоду (P < 0,001 для обох порівнянь) (рис. 7).
/11.jpg)
Автори дослідження дійшли висновку, що у пацієнтів з рецидивуючою фібриляцією передсердь лікування «таблетка в кишені» є ефективним та безпечним, з високим рівнем прихильності пацієнтів, низькою частотою небажаних явищ і помітним зниженням відвідувань відділень невідкладної допомоги і госпіталізацій.
Висновки
— Згідно з даними епідеміологічних досліджень, поширеність ФП становить 1 % у пацієнтів молодше від 60 років і досягає 6 % у старшій віковій групі. ФП призводить до підвищення ризику тромбоемболічних ускладнень, зокрема ішемічного інсульту, погіршує якість життя пацієнтів і призводить до зменшення очікуваної тривалості життя.
— ESC з діагностики та лікування ФП 2024 року рекомендує використання принципу AF-CARE: С — корекція факторів ризику і супутньої патології, А — профілактика інсульту і системної тромбоемболії, R — зменшення вираженості симптомів шляхом конт-ролю частоти шлуночкових скорочень і ритму, Е — обстеження і динамічне спостереження.
— Фармакологічний контроль ЧСС може досягатися бета-блокаторами, дигоксином, дилтіаземом і верапамілом або комбінованою терапією. Вибір, згідно з рекомендаціями ESC-2024, залежить від симптомів, наявності супутньої патології і потенційних побічних ефектів.
— Для відновлення синусового ритму ESC-2024, залежно від типу і тяжкості супутнього захворювання серцево-судинної системи, рекомендує вибір наступних ААП: флекаїніду, пропафенону, аміодарону, ібутиліду або вернакаланту. В Україні для фармакологічної кардіоверсії препаратами вибору є флекаїнід (пероральний), пропафенон та аміодарон.
— Флекаїнід має рекомендацію найвищого класу 1A для фармакологічної конверсії ритму при епізодах ФП, які потребують тривалого контролю для запобігання рецидиву та прогресуванню ФП, за винятком пацієнтів із порушеннями систолічної функції лівого шлуночка, тяжкою гіпертрофією лівого шлуночка або ішемічною хворобою серця (клас ІА).
— У рандомізованих контрольованих дослідженнях та метааналізі флекаїнід виявив перевагу над іншим ААП ІС класу, що застосовують при ФП. Ефективність конверсії ритму в групах флекаїніду становить від 50 до 90 %.
— У пацієнтів з рецидивуючою фібриляцією передсердь лікування флекаїнідом за принципом «таблетка в кишені» є ефективним та безпечним, з високим рівнем прихильності пацієнтів, низькою частотою небажаних явищ і помітним зниженням відвідувань відділень невідкладної допомоги і госпіталізацій.
/8.jpg)

/8_2.jpg)
/9.jpg)
/10.jpg)
/11.jpg)