Вступ
Артеріальна гіпертензія (АГ) є найпоширенішим хронічним захворюванням людини. Необхідність боротьби з АГ обумовлена тим, що вона є найважливішим чинником ризику порушень мозкового кровообігу, інфаркту міокарда, ураження судин, нирок, втрати зору, серцево-судинних захворювань і смертності та найпоширенішим захворюванням в Україні [1–5, 15]. Блокатори рецепторів ангіотензину (БРА) II є одним із лідерів серед п’яти класів антигіпертензивних препаратів першої лінії за органопротекторними властивостями та метаболічними ефектами. Унікальність дії телмісартану визначається низкою його особливих властивостей. По-перше, афінітет телмісартану до рецепторів ангіотензину II першого типу надзвичайно високий, а ступінь дисоціації дуже низький, що забезпечує більш повну й ефективну блокаду рецепторів. –Телмісартан серед інших БРА має один із найтриваліших періодів напіввиведення — понад 24 год. Крім того, для телмісартану характерний дуже високий ступінь проникнення в тканини, а також найбільший серед БРА об’єм розподілу у внутрішньому середовищі організму. У поєднанні з доброю переносимістю та безпечністю ці характеристики становлять основу забезпечення більш ефективного порівняно з іншими БРА конт–ролю артеріального тиску (AT), а також блокади ренін-альдостеронової системи у тканинах [13, 14].
Нещодавно в ряді експериментальних досліджень було доведено, що телмісартан, на відміну від інших блокаторів ангіотензину II, має часткову активність щодо Peroxisome proliferator-activated receptors (PPAR) гамма в терапевтичній дозі, рекомендованій для лікування АГ, і таким чином сприяє підвищенню інсуліночутливості [13, 14, 21, 22, 24, 25]. Увага до PPAR обумовлена їх ключовою роллю в регуляції жирового та карбогідратного метаболізму взагалі, а також у формуванні метаболічного синдрому (інсулінорезистентності) і цукрового діабету (ЦД) 2-го типу зокрема [13]. Доведено, що серед відомих БРА телмісартан має найвищий активуючий ефект щодо PPAR-гамма — у 20 разів більший, ніж кандесартан, ірбесартан, олмесартан, а також лосартан і його активний метаболіт [14, 22]. Показано, що конформаційна структура молекули телмісартану близька до структури глітазонів [21]. Здатність телмісартану активувати PPAR-гамма лише в 2 рази менша, ніж у специфічних агоністів цих рецепторів — піоглітазону та розиглітазону. Отже, телмісартан має подвійний механізм дії [13]. Маючи високу спорідненість до рецептора ангіотензину II (тип АТ1), через який реалізується його дія, препарат витісняє ангіотензин II із зв’язку з рецептором. Зв’язування має тривалий характер. Сприяючи зниженню рівня альдостерону в крові, телмісартан, проте, не впливає на рівень реніну та іонні канали, не пригнічує ангіотензинперетворюючий фермент (АПФ), який інактивує брадикінін [14]. При прийомі всередину в дозі 80 мг/добу препарат повністю блокує гіпертензивний ефект ангіо–тензину II [22]. Ефективна дія препарату триває понад 24 години й визначається через 48 годин. У пацієнтів з АГ телмісартан знижує систолічний та діастолічний АТ (САТ, ДАТ), не впливаючи на частоту серцевих скорочень (ЧСС) [14, 24]. За допомогою БРА першого типу телмісартан зменшує прояви АГ, клітинної проліферації, запалення, а також оксидативного стресу. З іншого боку, унаслідок активації PPAR-гамма препарат знижує рівень інсулінорезистентності, дисліпідемії, системного запалення, проліферації клітин і оксидативного стресу. Кінцевою реалізацією зазначених шляхів впливу телмісартану є гальмування процесу атерогенезу. Отже, використання лікарського препарату з подвійним механізмом дії, як у телмісартану, буде особливо ефективним у хворих із високим ризиком серцево-судинних захворювань і метаболічних порушень [13, 14, 21, 22, 24, 25].
Ще один препарат, який успішно використовується в лікуванні артеріальної гіпертензії, — це амлодипін. Амлодипін продемонстрував високу ефективність та позитивно впливав на прогноз у хворих із високим ризиком серцево-судинних ускладнень. Новим напрямком у фармакології є виділення ізомерів із рацемічної суміші. Амлодипін є рацемічною сполукою, що складається із рівних за пропорціями ізомерів (S і R). Показано, що S-амлодипін у 1000 разів сильніше зв’язується з дигідропіридиновими рецепторами, має антиангінальні та судинорозширюючі властивості. S-амлодипін має більшу фармакологічну активність та має більш тривалий період напіввиведення (до 49,5 год). У дослідженні SESA, присвяченому вивченню ефективності та безпечності S-амлодипіну, показана висока ефективність такої форми в дозі 2,5 та 5 мг. У частини хворих спостерігалися набряки при лікуванні рацемічним амлодипіном, але після переводу їх на S-амлодипін у 98,7 % набряки суттєво зменшилися. Особливістю S-амлодипіну є можливість застосування менших доз із таким же клінічним ефектом без побічних реакцій [26, 27].
Метою нашого дослідження було оцінити антигіпертензивний ефект генеричного препарату телмісартан (Хіпотел виробництва компанії «Кусум Фарм», Україна) як монотерапії або комбінації із S-амлодипіном (Семлопін виробництва компанії «Кусум Фарм», Україна) у пацієнтів із м’якою та помірною артеріальною гіпертензією.
Матеріали та методи
У дослідження було включено 40 пацієнтів із м’якою та помірною АГ (середній рівень офісного систолічного/діастолічного АТ — 155,88/92,60 ± 1,63/1,43 мм рт.ст.), ЧСС — 71,40 ± 1,29 уд/хв. Середній вік хворих становив 55,85 ± 2,09 (26–74) року.
Критерії включення в дослідження:
— чоловіки та жінки віком від 18 до 75 років;
— м’яка та помірна есенціальна артеріальна гіпертензія згідно з класифікацією ВООЗ (1999) (Міжнародного товариства з вивчення артеріальної гіпертензії) та Українського товариства кардіологів за умови, що в кінці семиденного періоду відміни всіх антигіпертензивних препаратів середні значення артеріального тиску, виміряного в першій половині дня в положенні сидячи, будуть такими: офісний систолічний артеріальний тиск — ≥ 140 мм рт.ст., але < 180 мм рт.ст., діастолічний артеріальний тиск — ≥ 90 мм рт.ст., але < 110 мм рт.ст.;
— відсутність критеріїв виключення.
Критеріями виключення були: ангіоневротичний набряк в анамнезі, гіперкаліємія (> 5,5 ммоль/л) або гіпокаліємія (< 3,5 ммоль/л), гостра серцева недостатність, порушення серцевого ритму (хронічна фібриляція передсердь, часта екстрасистолічна аритмія, шлуночкова або надшлуночкова тахікардія, тахікардія (ЧСС понад 100 уд/хв), порушення атріовентрикулярної провідності, або синусова брадикардія, або синдром слабкості синусового вузла, наявність вад серця, вагітність або лактація, злоякісний перебіг артеріальної гіпертензії, вторинна артеріальна гіпертензія, виражена артеріальна гіпотонія (САТ нижче від 90 мм рт.ст.), бронхіальна астма, декомпенсовані захворювання печінки (рівень аспартатамінотрансферази (АСТ), аланінамінотрансферази (АЛТ) вище від верхньої границі норми в 3 рази), гостра або хронічна ниркова недостатність (розрахункова швидкість клубочкової фільтрації (ШКФ) (за CKD-EPI) < 30 мл/хв), серцева недостатність II функціонального класу і вище (згідно з Нью-Йоркською класифікацією), інфаркт міокарда в анамнезі строком менше ніж 6 місяців до моменту включення в дослідження, гостре порушення мозкового кровообігу в анамнезі, наявність стенокардії напруження ІІІ–IV функціонального класу або вазоспастичної стенокардії, інфекційні та онкологічні захворювання, стани, що супроводжуються ендогенною депресією (чи наявністю депресивних станів у сім’ї), цукровий діабет, ожиріння (індекс маси тіла (ІМТ) > 40 кг/м2), виражені захворювання периферичних судин, синдром Рейно, стан після хірургічного втручання (менше від одного місяця), прийом стероїдних та нестероїдних протизапальних засобів, контрацептивів, значні психічні розлади, неможливість відмінити попередню антигіпертензивну терапію, участь в іншому дослідженні.
Після семиденного періоду відміни всіх медикаментозних засобів пацієнти проходили початкове обстеження та розподіл на групи методом сліпих конвертів залежно від призначеної антигіпертензивної терапії. У кінці періоду відміни оцінювали повторно критерії включення в дослідження. Якщо пацієнт відповідав критеріям включення і не мав критеріїв виключення, то відбувалася рандомізація пацієнта за схемою, наведеною на рис. 1.
/13-1.gif)
Усім пацієнтам на початку та в кінці лікування проводили такі дослідження: вимірювання маси тіла та зросту, розрахунок індексу маси тіла. Діагноз надлишкової ваги тіла або ожиріння встановлювали відповідно до критеріїв ВООЗ (1997). Надлишкову вагу тіла встановлювали при значенні ІМТ від 25 до 29,9 кг/м2, ожиріння I ступеня — ІМТ від 30 до 34,9 кг/м2, ожиріння II ступеня — ІМТ від 35 до 39,9 кг/м2, ожиріння III ступеня — ІМТ понад 40,0 кг/м2, проводили вимірювання офісного САТ, ДАТ та ЧСС, добове моніторування АТ (ДМАТ), визначення швидкості поширення пульсової хвилі по артеріях еластичного (ШППХе) та м’язового (ШППХм) типів, визначення центрального САТ, біохімічне дослідження крові (визначення рівнів калію, натрію, креатиніну, сечової кислоти, АЛТ, АСТ, білірубіну, глюкози), визначали ліпідний обмін, зокрема вміст загального холестерину (ХС), тригліцеридів, холестерину ліпопротеїнів високої щільності (ХС ЛПВЩ), холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ), холестерину ліпопротеїнів дуже низької щільності (ХС ЛПДНЩ), індекс атерогенності (ІА).
Вимірювання офісного САТ та ДАТ проводили на початку дослідження, після семиденної (у разі необхідності) відміни всіх антигіпертензивних препаратів та в кінці лікування. Вимірювали АТ у положенні сидячи тричі з інтервалом 1–2 хв. ЧСС визначали після другого вимірювання.
Індекс маси тіла визначали за формулою:
ІМТ = маса тіла/(ріст)2, кг/м2.
Методика добового моніторування артеріального тиску. ДМАТ проводили за допомогою апаратів АВРМ-04М (фірма «Медітек», Угорщина). При цьому вивчали такі показники: середньодобовий, денний, нічний систолічний АТ, середньодобовий, денний, нічний діастолічний АТ, ЧСС. При аналізі ДМАТ для САТ і ДАТ розраховували індекс часу, що характеризує часове перевантаження тиском протягом доби та визначається як відсоток вимірів АТ, що перевищує 140/90 мм рт.ст. вдень і 120/80 мм рт.ст. вночі. Також визначали індекс навантаження тиском (ІП), що є площею між кривою підвищеного АТ та лінією границі норми, а також індекс варіабельності (СВ), який обчислювали як стандартне відхилення величини АТ. Крім того, за допомогою програмного забезпечення вираховували добовий індекс (ДІ) —відсоток зниження нічного АТ порівняно з денним. Моніторування проводили в такому режимі: у денний час — кожні 15 хвилин, уночі (з 22:00 до 6:00) — кожні 30 хвилин. Хворі вели звичайний спосіб життя з побутовими фізичними й психоемоційними навантаженнями.
Індекс часу (навантаження тиском) розраховували як відсоток вимірів, що перевищують нормальні показники. Індекс часу для систолічного АТ вважається нормальним, якщо він не перевищує 20 %, а для діастолічного АТ — до 15 % (White, 1989). Динаміка індексу навантаження тиском дає змогу оцінити адекватність лікування.
При оцінці добового ритму АТ нормальним вважається зменшення АТ вночі під час сну на 10–20 % порівняно з денним періодом. Ступінь нічного зниження САТ та ДАТ, або добовий індекс, розраховували за формулою (окремо для САТ та ДАТ):
ДІ = (серАТд – серАТн) • 100 % / серАТд,
де серАТд — середньоденний АТ (САТ чи ДАТ), серАТн — середньонічний АТ (САТ чи ДАТ).
Оцінка добового ритму АТ:
а) нормальне зниження АТ вночі (dipper) — 10–20 %;
б) недостатнє зниження (non-dipper) — 0–10 %;
в) підвищений ступінь нічного зниження (hyper-dipper) — понад 20 %;
г) стійке підвищення АТ вночі (night-peaker) — нічний АТ більший від денного.
Доведено, що підвищений АТ протягом ночі супроводжується більшим ураженням органів-мішеней (гіпертрофія міокарда, серцева недостатність, гломерулосклероз та ниркова недостатність, ретинопатія та інше). Тривалі спостереження показали, що хворі з порушеним добовим ритмом АТ (non-dipper), особливо жінки, мають достовірно більший рівень серцево-судинних ускладнень.
Варіабельність АТ є важливою детермінантою ураження органів-мішеней. Крім того, існують непрямі докази, що збільшення варіабельності АТ несприятливо впливає на число серцево-судинних ускладнень та смертність. Варіабельність САТ та ДАТ розраховували як стандартне відхилення від середнього значення, тобто як коефіцієнт варіабельності середньої величини САТ і ДАТ за добу, день, ніч.
Біохімічні аналізи виконувалися в сертифікованій в Україні лабораторії «Сінево». Визначали рівень креатиніну, електролітів (калію та натрію), глюкози, загального ХС, тригліцеридів, ХС ліпопротеїнів високої щільності, ХС ліпопротеїнів низької щільності, ХС ліпопротеїнів дуже низької щільності сироватки крові. Кліренс креатиніну, що відображає ШКФ, розраховували за формулою Cockroft — Gault.
Ми оцінювали вплив терапії на показники еректильної функції в чоловіків за допомогою анкети МІЕД (Міжнародний індекс еректильної дисфункції).
Усі перераховані вище клінічні, лабораторні та функціонально-діагностичні обстеження проводили на початку дослідження та в кінці періоду лікування.
Клінічну ефективність лікування оцінювали шляхом порівняння динаміки клініко-лабораторних та функціонально-діагностичних показників у хворих на початку та в кінці лікування.
Статистичну обробку результатів проводили після створення баз даних у системах Microsoft Excel. Усі статистичні розрахунки проводили за допомогою програми SPSS 21. Достовірність різниці середніх між групами визначалася методом незалежного t-тесту для середніх. Порівняння динаміки показників на етапах лікування проводили за допомогою парного двовибіркового t-тесту для середніх. Кореляційний аналіз проводили після визначення характеру розподілу за Spearman.
Результати
Середній вік хворих становив 55,85 ± 2,09 року. Середня маса тіла становила 87,30 ± 2,77 кг. Середній ІМТ — 29,41 ± 0,63 кг/м2. Середні цифри офісного САТ та ДАТ на початку дослідження становили 155,90 ± 1,63 мм рт.ст. та 92,60 ± 1,43 мм рт.ст. відповідно. Середня офісна ЧСС — 71,40 ± 1,29 уд/хв. Середні рівні АТ при амбулаторному моніторуванні становили для САТ 139,37 ± 1,49 мм рт.ст., для ДАТ — 82,47 ± 1,84 мм рт.ст. Середня добова ЧСС — 71,38 ± 1,32 уд/хв. Основні клініко-демографічні показники пацієнтів подані в табл. 1.
Виконано аналіз структури призначення терапії. На початку 95 % хворих приймали монотерапію у вигляді Хіпотелу (телмісартану) 40 або 80 мг один раз на добу. Через 24 тижні 35 % пацієнтів залишилися на монотерапії, останні 65 % приймали подвійну комбіновану терапію Хіпотелом (телмісартаном) 40–80 мг із Семлопіном (S-амлодипіном) 2,5–5 мг або потрійну — з додаванням гідрохлортіазиду (ГХТ) 12,5 мг один раз на добу. Дані наведені на рис. 2, 3.
На фоні терапії Хіпотелом у загальній групі зниження офісного АТ на етапах 14 днів, 4 тижні, 8 тижнів та 24 тижні становило 14,0/7,7 мм рт.ст., 22,0/10,7 мм рт.ст., 25,5/13,5 мм рт.ст., 26,8/12,3 мм рт.ст. відповідно (р < 0,05) для всіх значень. Дані наведені на рис. 4.
Для ефективного зниження АТ необхідний підбір найбільш ефективних схем лікування. Для досягнення цільового рівня АТ у пацієнтів з АГ зазвичай необхідне призначення комбінованої терапії. Відповідно до сучасних рекомендацій з лікування АГ більшість пацієнтів потребують 2 або більше лікарських засобів для досягнення цільових рівнів АТ. При рівні офісного АТ 160/100 мм рт.ст. і вище рекомендовано відразу починати лікування з комбінованої антигіпертензивної терапії. Такі висновки були зроблені на основі результатів багатьох клінічних досліджень, що продемонстрували необхідність комбінованої терапії [17, 18]. Комбінація антигіпертензивних препаратів із взаємодоповнюючою дією підвищує ефективність та переносимість лікування порівняно з високими дозами, що застосовуються при монотерапії, сприяє зменшенню дозозалежних побічних реакцій, що спостерігалися при монотерапії високих доз, та синергізму плейотропних ефектів препаратів.
Ми проаналізували динаміку офісного САТ окремо в пацієнтів, які приймали монотерапію Хіпотелом, та в тих, які приймали Хіпотел у комбінації із Семлопіном або ГХТ. На фоні монотерапії Хіпотелом зниження офісного САТ на етапах 14 днів, 4 тижні, 8 тижнів та 24 тижні становило 14,0; 24,7; 25,8; 26,7 мм рт.ст. відповідно (р < 0,05) для всіх значень. Аналогічні дані були отримані й на фоні комбінованої терапії. Так, зниження офісного САТ на етапах 14 днів, 4 тижні, 8 тижнів та 24 тижні становило 14,3; 18,4; 24,1; 25,7 мм рт.ст. відповідно (р < 0,05) для всіх значень. Дані наведені на рис. 5.
Отже, можна стверджувати, що застосування Хіпотелу (телмісартану) як монотерапії або в комбінації із Семлопіном (S-амлодипіном) було ефективним у зниженні офісного АТ починаючи з 14-го дня терапії та протягом 6 місяців лікування.
/16-2.gif)
Ми оцінили динаміку АТ при добовому моніторуванні. Дані наведені на рис. 6, 7 та в табл. 2. Нами відмічено значне та достовірне зниження АТ як за весь період, так і за денний та нічний періоди. Так, зниження артеріального тиску при добовому моніторуванні на фоні прийому Хіпотелу через 24 тижні лікування становило за всю добу 15,7/9,3 мм рт.ст., за денний період — 15,3/9,2 мм рт.ст., за нічний період — 15,4/8,7 мм рт.ст. (р < 0,05) для всіх значень. ЧСС достовірно не змінилася: за всю добу ЧСС зменшилася на 1,55 уд/хв, за денний період — на 1,4 уд/хв, за нічний період — на 1 уд/хв. Достовірно знизився пульсовий АТ — як за всю добу, так і за денний та нічний періоди (табл. 2). Також знизився достовірно й максимальний САТ за всю добу, за денний та нічний періоди. За нічний період знизився достовірно й максимальний ДАТ та максимальний пульсовий АТ. Значним та достовірним було зниження індексів площі для САТ та ДАТ за всю добу, за денний та нічний періоди, що свідчить про добрий антигіпертензивний ефект Хіпотелу або при монотерапії 40–80 мг, або в комбінації із Семлопіном 2,5–5 мг на добу.
/17-1.gif)
При аналізі даних добового моніторування на фоні монотерапії Хіпотелом зниження САТ становило на етапі 8 тижнів за весь період 16,1 мм рт.ст., за денний період — 17,2 мм рт.ст., за нічний пе–ріод — 14,5 мм рт.ст. На етапі 24 тижні зниження САТ при добовому моніторуванні становило 17,6; 19,6 та 15,3 мм рт.ст. відповідно (р < 0,05) для усіх значень. При аналізі даних добового моніторування на фоні комбінованої терапії Хіпотелом із Семлопіном зниження САТ становило на етапі 8 тижнів за весь період 7,4 мм рт.ст., за денний період — 7,6 мм рт.ст., за нічний період — 3,9 мм рт.ст. (р < 0,05). На етапі 24 тижні зниження САТ при добовому моніторуванні становило 8,5; 8,0 та 5,4 мм рт.ст. (р < 0,05) для всього пе–ріоду, денного та нічного періоду –відповідно. –Різницю в зниженні АТ при добовому моніторуванні на фоні моно- та комбінованої терапії можна пояснити тим, що при комбінованій терапії пацієнти мали вищий рівень АТ із самого початку, він гірше піддавався лікуванню, що й потребувало призначення комбінованої антигіпертензивної терапії.
Досягнення цільового рівня АТ при офісному вимірюванні становило в цілому по групі 80 %, при монотерапії Хіпотелом у всіх 100 % пацієнтів було досягнуто цільовий рівень АТ, при комбінованій терапії Хіпотел плюс Семлопін — у 72 % пацієнтів. При добовому моніторуванні досягнення цільового АТ у цілому по групі становило 90 %, при монотерапії Хіпотелом — 93 %, а при комбінації Хіпотелу із Семлопіном — 80 % пацієнтів. Більш низькі показники в досягненні цільового рівня АТ на фоні комбінованої терапії можна пояснити тим, що ці пацієнти мали більш високий рівень АТ, а тому гірше піддавались терапії. Дані наведені на рис. 8, 9.
Нами не відмічено достовірної динаміки лабораторних показників протягом 24 тижнів лікування. Дані наведені в табл. 3.
/18-1.gif)
Ми оцінювали вплив терапії в групах спостереження на показники еректильної функції в чоловіків за допомогою анкети МІЕД. У дослідженні Р. Аranda зі співавт. у 2130 чоловіків з АГ вивчали поширеність ЕД та встановили, що 45,8 % чоловіків з АГ мали ЕД [5]. У дослідженні M. Doumas зі співавт. порівнювали поширеність еректильної дисфункції в гіпертензивних та нормотензивних чоловіків та встановили, що поширеність ЕД у чоловіків з АГ була 35,2 %, а в нормотензивних чоловіків — 14,1 % [9]. Деякі дослідження показують, що ішемічна хвороба серця та ЕД мають загальні фактори ризику. Так, у дослідженні А. Greenstein зі співавт. ЕД корелювала з кількістю закритих коронарних артерій [12]. В основі еректильного збудження лежить вивільнення оксиду азоту. Тому всі чинники, що впливають на вивільнення NO, можуть сприяти покращенню еректильної функції в чоловіків [9]. Тому ми вирішили дослідити, яким чином телмісартан у монотерапії або застосування комбінації з амлодипіном впливає на стан еректильної функції в чоловіків. Дані наведені в табл. 4. Нами не було виявлено достовірних змін еректильної функції в чоловіків, які брали участь у нашому дослідженні.
/19-1.gif)
Нами не відмічено серйозних побічних реакцій при прийомі Хіпотелу як при монотерапії, так і в комбінації із Семлопіном. Лише в 1 пацієнта (2,5 %) через 1 місяць лікування при монотерапії Хіпотелом 80 мг на добу виникли сонливість, запаморочення, біль в очах, відчуття оніміння в потилиці, що було пов’язано з неадекватним контролем АТ через 1 місяць терапії. Цільовий рівень АТ було досягнуто через 2 місяці лікування після додавання Семлопіну 5 мг.
Обговорення
Дане дослідження показало, що при прийомі 40–80 мг телмісартану (Хіпотел) як монотерапії або в комбінації із S-амлодипіном (Семлопін) 2,5–5 мг ефективно знижувався АТ як при офісному вимірюванні, так і при добовому моніторуванні. Переваги телмісартану в забезпеченні тривалого антигіпертензивного ефекту протягом доби були продемонстровані в численних клінічних дослідженнях, вони доводять позитивні антигіпертензивні ефекти телмісартану. У дослідженні PRISMA I та II проводили порівняння впливу телмісартану 80 мг та раміприлу 40 мг на рівень ранкового підйому АТ у пацієнтів із м’якою та помірною АГ за даними добового моніторування АТ. Було доведено, що телмісартан у дозі 80 мг на добу ефективніше знижував АТ, ніж раміприл 40 мг на добу. У дослідженні G. Barkis (2002) телмісартан продемонстрував кращий контроль АТ у нічний та в ранковий час в останні 6 годин перед прийомом наступної дози препарату [11].
Метааналіз ABPM довів переваги телмісартану в зниженні ранкового підйому систолічного АТ. Було досліджено 108 пацієнтів з АГ, яким призначався телмісартан у монотерапії або в комбінації з амлодипіном у ранковий або вечірній час. Пацієнти були поділені на 4 групи. ДМАТ було проведено на початку та через 8 тижнів лікування. У кінці лікування зниження САТ/ДАТ за даними добового моніторування в групах становило 29,94/16,32 мм рт.ст., 31,37/18,35 мм рт.ст., 29,49/17,30 мм рт.ст. та 25,80/15,51 мм рт.ст. і не відрізнялося між групами. Використання комбінації телмісартану з амлодипіном як у ранковий час, так і у вечірні години однаково ефективно знижувало АТ, а варіабельність АТ була меншою при прийомі комбінації телмісартану та амлодипіну у вечірні години [20].
Телмісартан не тільки забезпечує ефективний контроль АТ протягом 24 годин, а й має органопротекторні властивості та знижує серцево-судинний ризик у пацієнтів з АГ. Так, у 5-річному дослідженні ONTARGET (3,5–6 років) вивчали розвиток серцево-судинних подій у пацієнтів високого ризику, які приймали телмісартан, порівняно з хворими, яким призначався раміприл або їх комбінації. Уперше було доведено, що блокатори рецепторів ангіотензину II (телмісартан) так само ефективні, як і інгібітори АПФ (раміприл) у зниженні ризику серцево-судинних ускладнень. У телмісартану була краща переносимість порівняно з раміприлом. У дослідженнях INNOVATION, DETAIL, TRENDY, VI–VALDI був доведений нефропротекторний ефект телмісартану [6–8, 10, 15, 23].
У дослідженні INNOVATION телмісартан запобігав прогресуванню мікроальбумінурії в нормотензивних пацієнтів із цукровим діабетом 2-го типу в Японії. Телмісартан був безпечним та добре переносився пацієнтами [15]. У дослідженні DETAIL продемонстровано, що телмісартан добре конт–ролював артеріальний тиск та зменшував прогресування протеїнурії в пацієнтів із діабетичною нефропатією. Порівнювали вплив прийому 40–80 мг телмісартану та 10–20 мг еналаприлу на частоту виникнення ниркових подій у пацієнтів із цукровим діабетом 2-го типу та м’якою й помірною АГ з наявною альбумінурією. Нефропротекторний ефект обох препаратів був порівнянний та асоціювався зі зменшенням кількості летальних випадків [6]. У дослідженні TRENDY вивчали вплив телмісартану порівняно з раміприлом на рівень адипонектину та ендотеліальну функцію ниркових судин у пацієнтів із цукровим діабетом 2-го типу без альбумінурії. Рівень адипонектину обернено корелював із рівнем АТ у пацієнтів із ЦД 2-го типу. Доведено, що ендотеліальна функція, яка була оцінена за рівнем оксиду азоту, покращувалася після блокади ренін-ангіотензинової системи [8, 23]. У дослідженні VIVALDI вивчали вплив телмісартану порівняно з валсартаном на рівень протеїнурії в пацієнтів з АГ та цукровим діабетом 2-го типу з нефропатією. Доведено однаковий нефропротекторний ефект щодо впливу на протеїнурію в телмісартану й валсартану та на рівень ШКФ протягом 12 місяців. Більший ренопротекторний ефект спостерігався в пацієнтів із кращим контролем АТ. Не було достовірних змін рівня С-реактивного білка в обох групах через 12 місяців [7, 10].
Також визначені нові показання для телмісартану Європейською агенцією з лікарських засобів для лікування ішемічної хвороби серця, інсульту, захворювань периферійних артерій, ЦД 2-го типу для зниження серцево-судинного ризику. У дослідженні АТТЕМРТ-CVD, що тривало 3 роки, телмісартан порівняно з іншими антигіпертензивними препаратами достовірно знижував співвідношення альбумін/креатинін сечі, впливав на рівень –натрійуретичного пептиду крові, які є незалежними факторами ризику розвитку серцево-судинних подій [2, 19].
У дослідженні ARAMIS вивчали вплив телмісартану 20, 40 і 80 мг у 1039 пацієнтів з ізольованою АГ порівняно з ГХТ 12,5 мг або плацебо. Усі дози телмісартану були ефективні в зниженні АТ та порівнянні з ГХТ 12,5 мг, а переносимість телмісартану була порівнянною з плацебо. Зниження САТ при прийомі в дозі 20 мг телмісартану становило через 4 тижні терапії 15,6 мм рт.ст., а 40 мг телмісартану — 17,9 мм рт.ст., 80 мг телмісартану — 16,9 мм рт.ст. На фоні ГХТ 12,5 мг зниження САТ становило 15,7 мм рт.ст. Досягнення цільового рівня САТ становило 46,6 % при прийомі 20 мг телмісартану, 51,7 % — при прийомі 40 мг телмісартану, 53,9 % — при прийомі 80 мг телмісартану та 42,7 % — при прийомі ГХТ 12,5 мг, що достовірно менше порівняно з телмісартаном 80 мг [16].
Є.П. Свіщенко зі співавт. вивчали метаболічні та органопротекторні властивості телмісартану в 30 пацієнтів з артеріальною гіпертензією протягом 6 місяців. Так, зниження середньодобових показників для САТ відбувалося з 148,3 ± 2,5 мм рт.ст. до 134,9 ± 2,5 мм рт.ст., а для ДАТ — з 87,6 ± 1,8 мм рт.ст. до 79,7 ± 1,3 мм рт.ст. (р < 0,05), досягнення цільових рівнів АТ спостерігалось у 73 % пацієнтів. У пацієнтів із зниженою швидкістю клубочкової фільтрації — менше від 60 мл/хв на фоні прийому телмісартану відбулося достовірне підвищення ШКФ [1].
У 2002–2003 роках в Україні було проведене перше відкрите багатоцентрове дослідження з вивчення ефективності та безпечності оригінального телмісартану в пацієнтів із різним ступенем підвищення АТ. 490 пацієнтів з АГ були включені в 3-місячне дослідження. Телмісартан призначався в початковій дозі 40 мг один раз на добу з наступним збільшенням дози при необхідності до 80 мг (середня добова доза становила 75 мг). Якщо монотерапія була неефективною, після 4-го тижня додавали ГХТ. Середній вік хворих становив 54,70 ± 0,56 року, середні цифри офісного САТ — 176,8 ± 1,27 мм рт.ст., ДАТ — 104,00 ± 0,65 мм рт.ст. Через 3 місяці середнє зниження САТ становило 32,6 мм рт.ст., ДАТ — 18 мм рт.ст., ЧСС — 7,3 уд/хв (p < 0,001). Цільовий рівень АТ (< 140/90 мм рт.ст.) було досягнуто в 76,4 % пацієнтів. Було зареєстровано тільки 3 (0,54 %) випадки побічних реакцій у вигляді головного болю, свербіння шкіри та діареї. За даними літератури, переносимість телмісартану порівнюється з такою в плацебо. Кількість пацієнтів, у яких вдавалося досягти цільового рівня АТ на фоні прийому телмісартану, коливається від 43 до 82 % [4].
У 2006–2007 роках нами було проведене дослідження порівняльної ефективності оригінального телмісартану та фозиноприлу в пацієнтів із м’якою та помірною АГ й метаболічним синдромом. Були обстежені 73 пацієнти з АГ та метаболічним синдромом. Зменшення артеріального тиску як при офісному вимірюванні, так і при добовому моніторуванні після 6 місяців лікування було достовірним, але не відрізнялося в групах пацієнтів. Так, зменшення офісного САТ становило 28 мм рт.ст. при лікуванні телмісартаном та 27,5 мм рт.ст. при лікуванні фозиноприлом, зменшення офісного ДАД становило 11,5 та 12,2 мм рт.ст. відповідно. Зменшення середньодобового САТ становило 17,41 та 16,44 мм рт.ст. на фоні лікування телмісартаном та фозиноприлом відповідно, ДАТ зменшилось на 9,94 та 10,10 мм рт.ст. відповідно. Зміни варіабельності артеріального тиску та ЧСС в обох групах були недостовірними. Отже, ми бачимо, що ефективність генеричного телмісартану (Хіпотел) в нашому дослідженні порівнянна з ефективністю оригінального телмісартану [3].
Висновки
1. Телмісартан (Хіпотел) ефективно знижує артеріальний тиск як при офісному вимірюванні, так і при добовому моніторуванні протягом 24 тижнів лікування в пацієнтів із м’якою та помірною артеріальною гіпертензією.
2. На фоні терапії Хіпотелом у загальній групі зниження офісного АТ на етапах 14 днів, 4 тижні, 8 тижнів та 24 тижні становило 14,0/7,7 мм рт.ст., 22,0/10,7 мм рт.ст., 25,5/13,5 мм рт.ст., 26,8/12,3 мм рт.ст. відповідно (р < 0,05) для всіх значень.
3. На фоні монотерапії Хіпотелом зниження офісного САТ на етапах 14 днів, 4 тижні, 8 тижнів та 24 тижні становило 14,0; 24,7; 25,8; 26,7 мм рт.ст. відповідно (р < 0,05) для усіх значень.
4. На фоні комбінованої терапії Хіпотелом із Семлопіном зниження офісного САТ на етапах 14 днів, 4 тижні, 8 тижнів та 24 тижні становило 14,3; 18,4; 24,1 і 25,7 мм рт.ст. відповідно (р < 0,05) для всіх значень.
5. Зниження артеріального тиску при добовому моніторуванні на фоні прийому Хіпотелу через 24 тижні лікування становило за весь період 15,7/9,3 мм рт.ст., за денний період — 15,3/9,2 мм рт.ст., за нічний період — 15,4/8,7 мм рт.ст. (р < 0,05) для всіх значень.
6. Досягнення цільового АТ при офісному вимірюванні становило 80 %, при добовому моніторуванні — 90 %. При монотерапії Хіпотелом досягнення цільового АТ становило 100 % при офісному вимірюванні та 93 % при добовому моніторуванні, при комбінованій терапії досягнення цільового АТ становило 72 % при офісному вимірюванні та 80 % — при добовому моніторуванні.
7. Частота розвитку побічних реакцій становила 2,5 %.
8. Хіпотел як у монотерапії, так і в комбінації із Семлопіном добре переносився хворими.
Отже, можна стверджувати, що телмісартан (Хіпотел) як монотерапія або в комбінації із S-амло–дипіном (Семлопін) при призначенні в пацієнтів з АГ м’якого та помірного ступеня дозволяє ефективно знижувати як офісний АТ, так і АТ протягом 24 годин та може покращувати прогноз у пацієнтів з АГ.
Конфлікт інтересів. Не заявлений.
Список литературы
1. Свіщенко Є.П., Міщенко Л.А., Мхітарян Л.С. та ін. Метаболічні та органопротекторні властивості телмісартану в пацієнтів із гіпертонічною хворобою // Артеріальна гіпертензія. — 2014. — № 6. — С. 33-38.
2. Селюк М.Н. Телмисартан в лечении артериальной гипертензии: мы можем позволить себе лучшее // Здоров’я України. — 2016. — № 5. — С. 45.
3. Сиренко Ю.Н., Рековец О.Л. Антигипертензивная эффективность и безопасность телмисартана (микардиса) при артериальной гипертензии: первые результаты проспективного многоцентрового исследования в Украине // Український кардіологічний журнал. — 2003. — № 5. — С. 43-50.
4. Сіренко Ю.М., Рековець О.Л. Лікування артеріальної гіпертензії та метаболічних порушень: значення подвійного ефекту телмісартану для профілактики розвитку цукрового діабету // Ліки України. — 2005. — № 4. — С. 1-7.
5. Aranda P., Ruilope L.M., Calvo C. et al. Erectile dysfunction in essential arterial hypertension and effects of sildenafil: results of a Spanish national study // Am. J. Hypertens. — 2004. — Vol. 17(2). — P. 139-145.
6. Barnett A.H. Preventing renal complications in diabetic patients: the Diabetics Exposed to Telmisartan And enalaprIL (DETAIL) study // Acta Diabetol. — 2005. — Vol. 42, –Suppl. 1. — S42-49.
7. Böger R.H., Schwedhelm E., Maas R., Quispe-Bravo S., Skamira C. ADMA and oxidative stress may relate to the progression of renal disease: rationale and design of the VI–VALDI study // Vasc. Med. — 2005. — Vol. 10, –Suppl. 1. — S. 97-102.
8. Delles C., Raff U., Mimran A. еt al. Effects of telmisartan and ramipril on adiponectin and blood pressure in patients with type 2 diabetes (TRENDY) // Am. J. Hypertens. — 2008. — Vol. 21(12). — P. 1330-1336.
9. Doumas M., Tsakiris A., Douma S. et al. Factors affecting the increased prevalence of erectile dysfunction in Greek hypertensive compared with normotensive subjects // J. Androl. — 2006. — Vol. 27(3). — P. 469-477.
10. Galle J., Schwedhelm E., Pinnetti S., Böger R.H., Wanner C.; VIVALDI investigators. Antiproteinuric effects of angiotensin receptor blockers: telmisartan versus valsartan in hypertensive patients with type 2 diabetes mellitus and overt nephropathy // Nephrol. Dial Transplant. — 2008 — Vol. 23(10) — P. 3174-3183.
11. Gosse P., Schumacher H. Effect of telmisartan vs. ramipril on dipping status and blood pressure variability: pooled analysis of the PRISMA studies // Hypertens. Res. — 2014. — Vol. 37(2). — P. 151-157.
12. Greenstein A., Chen J., Miller H. et al. Does severity of ischemic coronary disease correlate with erectile function? // Int. J. Impot. Res. — 1997. — Vol. 9(3). — P. 123-126.
13. Kintscher U., Lyon C.J., Law R.E. Angiotensin II, PPAR-gamma and atherosclerosis // Front. Biosci. — 2004. — Vol. 1. — P. 359-369.
14. Kota B.P., Huang T.H., Roufogalis B.D. An overview on biological mechanisms of PPARs // Pharmacol. Res. — 2005. — Vol. 51. — P. 85-94.
15. Makino H., Haneda M., Babazono T. еt al. INNOVATION Study Group. Microalbuminuria reduction with telmisartan in normotensive and hypertensive Japanese patients with type 2 diabetes: a post-hoc analysis of The Incipient to Overt: Angiotensin II Blocker, Telmisartan, Investigation on Type 2 Diabetic Nephropathy (INNOVATION) study // Hypertens. Res. — 2008 — Vol. 31(4). — P. 657-664.
16. Manolis A.J., Reid J.L., de Zeeuw D., Murphy M.B., Seewaldt-Becker E., Köster J.; ARAMIS Study Group. Angiotensin II receptor antagonist telmisartan in isolated systolic hypertension (ARAMIS) study: efficacy and safety of telmisartan 20, 40 or 80 mg versus hydrochlorothiazide 12.5 mg or placebo // J. Hypertens. — 2004. — Vol. 22(5). — P. 1033-1037.
17. Mancia G., De Backer G., Dominiczak A. et al. 2007 Guidelines for the Management of arterial hypertension. The task force for the management of arterial hypertension of the European Society of Hypertension and of the European Society of Cardio–logy // J. Hypertension. — 2007. — Vol. 25. — P. 1105-1187.
18. Mancia G., Laurent S., Agabiti-Rosei E. et al. Reapparaisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document // J. Hypertens. — 2009. — Vol. 27. — P. 2121-2158.
19. Ogawa H., Soejima H., Matsui K. еt al.; ATTEMPT-CVD investigators. A trial of telmisartan prevention of cardiovascular diseases (ATTEMPT-CVD): Biomarker study // Eur. J. Prev. Cardiol. — 2016 — Vol. 23(9) — P. 913-921
20. Peng G.C., Wang Y.F., Xiao Y. еt al. Blood pressure lo–wering efficacy of telmisartan and amlodipine taking on the mor–ning or at bedtime: ABPM results // Zhonghua Xin Xue Guan Bing Za Zhi. — 2013 — Vol. 41(6) — P. 484-487.
21. Raji A., Seely E.W., Bekins S.A. et al. Rosiglitazone improves insulin sensitivity and lowers blood pressure in hypertensive patients // Diabetes Care. — 2003. — Vol. 26. — Р. 172-178.
22. Schiffrin E.L., Amiri F., Benkirane K., Iglarz M., Diep Q.N. Peroxisome proliferator-activated receptors: vascular and cardiac effects in hypertension // Hypertension. — 2003. — Vol. 42. — P. 664-668.
23. Schmieder R.E. Endothelial dysfunction: how can one intervene at the beginning of the cardiovascular continuum? (TRENDY) // J. Hypertens. Suppl. — 2006. — Vol. 24(2). — S31-35.
24. Schupp M., Janke J., Clasen R., Unger T., Kintscher U. Angiotensin type 1 receptor blockers induce peroxisome proliferator-activated receptor-gamma activity // Circulation. — 2004. — Vol. 4. — P. 2054-2057.
25. Yamagishi S., Takeuchi M. Telmisartan is a promi–sing cardiometabolic sartan due to its unique PPAR-gamma-inducing property // Med. Hypotheses. — 2005. — Vol. 64. — P. 476-478.
26. Park C.G., Ahn T.H., Cho E.J. еt al. Comparison of the Efficacy and Safety of Fixed-dose S-Amlodipine/Telmisartan and Telmisartan in Hypertensive Patients Inadequately Controlled with Telmisartan: A Randomized, Double-blind, Multicenter Study // Clin. Ther. — 2016. — Vol. 38(10). — P. 2185-2194.
27. Ihm S.H., Jeon H.K., Cha T.J. еt al. Efficacy and safety of two fixed-dose combinations of S-amlodipine and telmisartan (CKD-828) versus S-amlodipine monotherapy in patients with hypertension inadequately controlled using S-amlodipine monothe–rapy: an 8-week, multicenter, randomized, double-blind, Phase III clinical study // Drug Des. Devel. Ther. — 2016. — Vol. 10. — Р. 3817-3826.

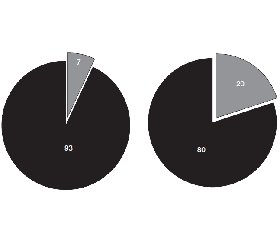
/13-1.gif)
/15-1.gif)
/15-2.gif)
/16-1.gif)
/16-2.gif)
/17-1.gif)
/18-2.gif)
/18-1.gif)
/19-1.gif)