Международный неврологический журнал 4(4) 2005
Вернуться к номеру
Сучасні підходи до нейропротекції при оперативних втручаннях на сонних артеріях
Авторы: Пшик С.С., Боженко Н.Л., Пшик Р.С. Кафедра неврології ЛДМУ ім. Данила Галицького
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Розглянуто ефективність препарату Прамістар для захисту мозку при оперативних втручаннях на екстракраніальних ділянках сонних артерій. Прамістар підвищує терапевтичну ефективність схем лікування церебральних дизгемій, зумовлених стенотичними ураженнями ВСА. Зазначені тенденції клінічної ефективності Прамістару дозволяють рекомендувати включення цього препарату у комплекс ведення хворих при оперативних втручаннях на ВСА та в післяопераційному періоді.
Проблема цереброваскулярної патології займає важливе місце в сучасній неврологічній практиці. Судинні захворювання головного мозку (транзиторні ішемічні атаки, інсульти) становлять від 30 до 50% захворювань серцево-судинної системи. За даними ВООЗ, смертність від інсультів складає 12-15% загальної смертності й стоїть після захворювань серця та злоякісних пухлин. Протягом року після ГПМК помирає до 40% хворих, лише 18-20% повертаються до праці, решта лишаються інвалідами. В Україні щорічно реєструється 125-175 тисяч інсультів. Така ж тенденція щодо росту цереброваскулярних захворювань (ЦВЗ) спостерігається й у Львівській області (рис. 1)
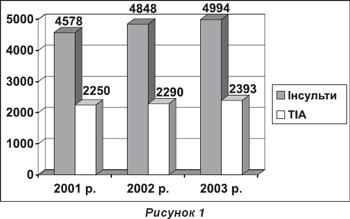
Відповідно, питання профілактики та лікування ЦВЗ мають надзвичайно важливе медичне та соціальне значення. Хірургічна корекція сонних артерій при їх оклюзивно-стенотичних ураженнях є загальновизнаним ефективним профілактичним методом у хворих з транзиторними ішемічними атаками. Суперечливими є думки спеціалістів щодо необхідності оперативного втручання у хворих, які перенесли ішемічний інсульт. Оперативне втручання скероване в таких випадках на профілактику повторних порушень мозкового кровообігу, а також на покращання кровопостачання головного мозку. Позитивним наслідком цього є зменшення неврологічного дефіциту в післяопераційному періоді.
Основними патогенетичними механізмами негативного впливу на паренхіму мозку хворих із ЦВЗ при ураженні екстракраніальних відділів сонних артерій є:
— виникнення турбулентного току крові в місцях стенозування магістральних артерій голови, що призводить до розвитку дефіциту кровотоку в дистальних відділах судин і басейні кровопостачання, що особливо виражено за недостатності кровопостачання при ненормальному ході сполучних артерій вілізієвого кола;
— формування синдрому обкрадання інтракраніальних судин з перерозподілом кровопостачання на користь ішемізованої ділянки мозку та подальшими дисциркуляторними розладами в зоні анатомічно незмінної васкуляризації;
— розвиток steal-синдрому при стенозуванні хребцевих та підключичних артерій з транзиторним дефіцитом у вертебробазилярному басейні;
— виникнення неповноцінності перфузії відповідного басейну при змінах системного артеріального тиску;
— утворення мікротромбів у пристінкових шарах внаслідок турбулентного кровотоку з вторинною хронічною негативною зміною реологічних характеристик крові, що тече до мозку. Мікроемболи, що утворюються, ведуть до спазму судин мікроциркулярного русла, а у важких випадках — до їх закупорки;
— вторинні розлади церебральної гемодинаміки на відстані від ураженого басейну внаслідок ішемізації ангіотонічних вегетативних центрів, дисфункція яких призводить до розладів церебральної гемодинаміки;
— при гострій церебральній ішемії, незалежно від причин, виникає порушення ауторегуляції церебральних артеріальних судин з неможливістю підтримання надалі адекватного рівня перфузії ураженої ділянки та подальшими вторинними змінами центральної гемодинаміки.
Враховуючи основні механізми патологічних змін церебральної гемодинаміки, можна зробити висновок, що основним завданням щодо ведення хворих є збереження та відновлення інтеграції мозкових структур, запобігання гіперперфузійному синдрому, нормалізація гемодинаміки, підтримання адекватного нейрометаболізму, профілактика тромбоемболічних ускладнень із застосуванням ліків, що мають нейрометаболічну, антиоксидантну, протиішемічну та вазотропну дію.
У прогресуванні ішемічного пошкодження головного мозку мають значення наступні фактори:
— гіпоксія мозкової тканини, порушення утилізації кисню, що поступає в недостатній кількості;
— некроз нейроцитів;
— активація процесів ПОЛ, що призводить до деструкції лізосомальних мембран;
— розлад обміну нейромедіаторів через розбалансування функції нейроцитів медіодиенцефальних структур;
— розлади біохімізму проведення електричного імпульсу до нервових волокон внаслідок вторинних вазогенних дизметаболічних розладів;
— порушення процесів транспорту Са+2 (відтік К+ з клітин, притік Na+, Cl-, Ca+2) призводить до деполяризації нейронних мембран, що сприяє звільненню у свою чергу збуджених нейротрансмітерів, які викликають нейротоксичний ефект та притік Ca+1 у нейрони. Внутрішньоклітинне накопичення Ca+1 викликає перевантаження мітохондрій та призводить до посилення катаболічних процесів.
На даному етапі не існує чітко окреслених методологічно-тактичних рекомендацій щодо ведення хворих при оперативному втручанні на сонних артеріях. Різні школи дотримуються різних схем.
В експериментальних роботах (В.Н. Клименко, І.Ф. Беленічев, 1993 р., Н.Ш. Аврущенко, 1991 р., М.О. Самійло, 1985 р.) встановлено, що навіть тимчасове виключення кровотоку в сонних артеріях, навіть при добре розвинених колатеральних судинах, не проходить безслідно для головного мозку, хоча може проявлятись лише субклінічно та біохімічно у вигляді компенсованого ішемічного пошкодження.
Найбільший інтерес клініцистів у зв'язку з перевагою проявів спрямований на групу нейротропних засобів, що ще називають «ліками ХХІ століття», засобів, які мають своєрідний спектр фармакологічної активності в сполученні з оптимальними характеристиками безпеки та надзвичайно широкими можливостями застосування, — ноотропів.
Головна принципова особливість дії цих препаратів — вплив на біохімічні процеси, що лежать в основі реалізації інтелектуально-мнестичних функцій, тобто регуляцію пізнавальної діяльності, навчання, пам'яті, а також вплив на процеси порушення адаптаційно-компенсаторних механізмів в ситуації довготривалого психоемоційного стресу. Провідне місце серед фармакологічних ефектів ноотропів посідають церебропротекторний та стресзахисний.
Найважливішими механізмами дії ноотропів є їх вплив на:
1) біосинаптичні процеси в мозку, тобто стимуляція процесів біосинтезу білкових структур у різних регіонах ЦНС;
2) енергетичні процеси в мозку, тобто поліпшення процесів енергозабезпечення, тканинного дихання, накопичення макроергічних сполук;
3) нейромедіаторні процеси в мозку, тобто нормалізація порушеного при різних негативних впливах балансу нейромедіаторів,
4) на кровопостачання мозку шляхом реалізації захисного впливу на судинну стінку, гальмування реакції тромбоутворення, нормалізації в'язкості крові та ін.
Ноотропи — це лікарські засоби, здатні виявляти пряму активуючу дію на процеси навчання, пам'яті, розумову діяльність, підвищувати стійкість мозку до будь-якого агресивного впливу та покращувати якість комунікаційного життя хворих (ВООЗ, 1991 р.)
Ноотропи впливають на різні ланки функціонально-метаболічних процесів у ЦНС, також на регулювання цими процесами психосоматичних та психоемоційних станів, а отже, на все різноманіття вищих психічних функцій.
Доцільним є застосування медикаментів вазотропної, метаболічної, антитромбоцитарної та антиоксидантної дії. З метою протиішемічного, нейрометаболічного захисту мозку ми використовували в комплексі ведення хворих при оперативному втручанні на сонних артеріях у доопераційній та післяопераційній підготовці ноотропний препарат «нового покоління», що з'явився в Україні з 2002 р., Прамістар (прамірацетам) фірми «Берлін-Хемі».
Прамістару притаманна мнемотропна, антидепресивна, антиастенічна, психостимулююча, транквілізуюча, адаптогенна, стресопротекторна, вазовегетативна дія, він сприяє підвищенню стійкості мозку до різних екстремальних впливів, покращує гемореологічні показники.
Механізм дії Прамістару включає:
1. Активацію синаптосомальної системи високоафінного захоплення холіну, що призводить до активації холінергічних процесів у мозку, тим самим стимулюючи біосинтез NO та покращуючи інтелектуально-мнестичні функції;
2. Інгібування активності нейропептидаз, що призводить до накопичення нейропептидів пам'яті в мозку, покращуючи інтелектуально-мнестичні функції;
3. Стимулюючий вплив на гіпокамп, ретикулярну фармацію, що збільшує рівень вазопресину;
4. Стимуляцію пресинаптичних адренергічних процесів, що призводить до збільшення мефетаміну та викликає антидепресивну дію.
Прамістар, на відміну від інших ноотропів, вибірково активує холінергічну нейромедіаторну систему мозку шляхом стимуляції процесів високоафінного зворотного захоплення холіну й, відповідно, збільшення його синаптичної активної концентрації. Цей ефект спостерігається тільки в нейронах гіпокампу.
Відомо, що холінергічна система в цілому й структури гіпокампу зокрема відіграють провідну роль у формуванні різних типів пам'яті, забезпеченні кірково-підкіркових зв'язків, реалізації функцій навчання, орієнтування. Не підлягає сумніву істотна роль холінергічної системи в реалізації стрес-індукованих порушень вищих психічних функцій. Отже, Прамістар — єдиний з усіх ноотропів, що має «точковий» вибірковий ефект впливу на провідні механізми старіння мозку та розвитку хронічного стресу в ЦНС, у результаті чого забезпечується селективна захисна дія для найбільш вразливих структур мозку, реалізується найважливіша умова фармакопрофілактичного ефекту.
Крім того, під впливом підвищених синаптичних концентрацій ацетилхоліну збільшується синтез оксиду азоту — речовини, що відіграє важливу роль у процесах пам'яті.
Ще однією специфічною стороною дії Прамістару є його вплив на нейропептидну медіацію, а саме на блокування ферментів нейропептидаз, у результаті чого відбувається підвищення концентрації вазопресину та кортикостерону в плазмі, тобто нейропептидів, що відіграють провідну роль у забезпеченні процесів пам'яті та навчання. Стимулюючи фізіологічні механізми нейропептидної медіації, прамірацетам має також захисний потенціал, що перешкоджає прогресуванню розладів, які лежать в основі розвитку цереброваскулярної патології.
Необхідно підкреслити, що аналогічного механізму дії не має жоден інший ноотропний препарат. Нарешті, ще одним важливим аспектом дії Прамістару є його антидепресивний ефект.
Отже, унікальність дії прамірацетаму полягає як в окремих сторонах його фармакологічного ефекту, так і в його комплексності, що виділяє даний препарат серед інших ноотропів.
Враховуючи все вищесказане, можна обгрунтувати можливість застосування Прамістару в комплексі лікування церебральних дизгемій, зумовлених атеросклеротичним ураженням екстракраніальних ділянок внутрішніх сонних артерій.
Обстежено 47 хворих (жінок 24, чоловіків 23) віком від 37 до 71 року, що проходили лікування у відділі хірургії судин ЛОКЛ. Тривалість хвороби становила від 2 до 5-7 років. Розподіл хворих за клінічними проявами представлено на рис. 2.
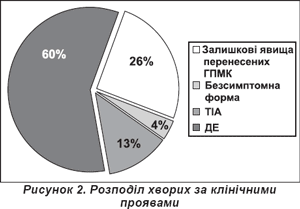
Контрольну групу складали 11 пацієнтів відповідного віку з аналогічними проявами, у комплекс терапії яким Прамістар не вводили.
Усім хворим проведено до операції УЗДГ та дуплексне сканування внутрішніх сонних артерій, комп'ютерну томографію головного мозку, частинні МРТ, консультації окуліста. У стаціонарі всіх хворих оглядали судинний хірург та невролог. Під час клінічної оцінки відзначено хорошу переносимість Прамістару.
Результати лікування подано в табл. 1.
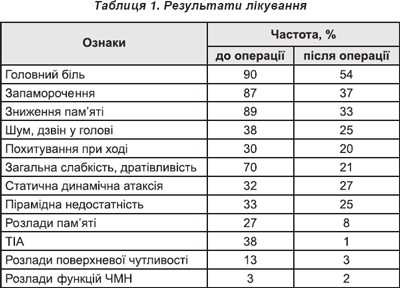
Після завершення операції хворих обов'язково переводили в блок інтенсивної терапії. Протягом доби проводили постійний моніторинг пульсу, артеріального тиску, ЕКГ, сатурації киснем. Динамічного контролю потребував неврологічний статус пацієнта. Огляди проводили через 3, 6, 12 та 24 години після операції. Хворих мобілізували швидко, дозволяючи сідати в спеціальних панчохах для профілактики тромбоемболії в першій половині наступного дня, вставати при відсутності виражених парезів — у другій половині того ж дня, стаціонарне спостереження проводилося протягом 5-7 днів.
Післяопераційні ускладнення вимагали корекції післяопераційної тактики ведення хворого. Враховуючи спільність причин та проявів, післяопераційні ускладнення поділили на декілька груп. Найбільш важким ускладненням, що й визначає в основному результати хірургічного лікування, є післяопераційна церебральна ішемія. В одного хворого констатовано наростання неврологічного дефіциту (воно було минаючим). Показане медикаментозне лікування, спрямоване на покращання мозкового кровообігу та запобігання подальшого тромбоутворення (введення Рефортану, L-лізину есцинату, дільцерену, кардонату, вітамінів С та Е, фраксипарину).
Профілактика ішемічних ускладнень потребує проведення ряду предопераційних та інтраопераційних заходів. При передопераційному обстеженні хворих особливу увагу звертали на показники коагулограми, гематокриту, проводячи корекцію порушень. Важливим вважаємо визначення шляхів колатерального кровообігу та тестування на толерантність мозку до оклюзії гомолатеральної сонної артерії за допомогою електроенцефалографії, доплерографії. Під час операцій доцільним є проведення моніторингу ЛШК по СМА під час перетискання сонних артерій. Обов'язково проводимо захист мозку від гіпоксії, моніторинг системної гемодинаміки та оксигенації крові.
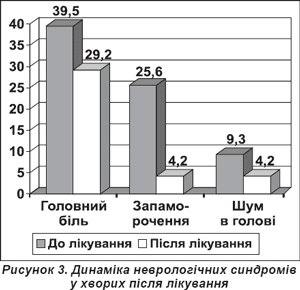
Після лікування стан покращився в 92% хворих, при цьому значне покращання вірогідно частіше відзначали хворі, у комплекс лікування яких входив Прамістар. Хворі відзначали зменшення болів голови, запаморочень, зниження пам'яті, шуму в голові, атактичних розладів, загальної слабості та депресивних проявів. У контрольній групі покращання показників спостерігалося в меншій мірі.
Динаміка змін стану хворих після лікування подана в табл. 2.
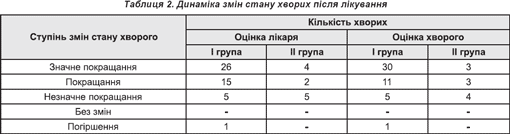
Із зазначених інструкцією побічних дій Прамістару лише у 5 хворих спостерігалось безсоння, що імовірно було пов'язано із пізнім вечірнім прийомом препарату, та підвищення збудливості у одного хворого.
Усім хворим у комлекс лікування, окрім класичної схеми, призначали Прамістар в дозі 150 мг х 2 рази на добу за 3-5 днів до операції. Добова доза препарату поступово підвищувалася до 1200 мг у 2 прийоми. Підтримуючу дозу 1200 мг у 2 прийоми усі хворі продовжували застосовувати ще протягом 1 місяця.
Аналіз ефективності застосування Прамістару засвідчив, що:
— лікування повинно бути комплексним і достатньо тривалим, включати передопераційну підготовку;
— Прамістар — ефективний препарат медикаментозного захисту мозку при оперативних втручаннях на екстракраніальних ділянках сонних артерій;
— застосування Прамістару сприяє повнішому відновленню втрачених функцій та зменшенню післяоперативних ускладнень;
— особливо ефективним є Прамістар щодо покращання когнітивних функцій, зменшення запаморочення, головних болів, збільшення моторної активності, зниження депресивних проявів у хворих з атеросклеротичною ДЕ;
— Прамістар підвищує терапевтичну ефективність схем лікування церебральних дизгемій, зумовлених стенотичними ураженнями ВСА.
Зазначені тенденції клінічної ефективності Прамістару дозволяють рекомендувати цей препарат у комплекс ведення хворих при оперативних втручаннях на ВСА, та в післяопераційному періоді.
1. Бурчинский С.Г. Прамирацетам — ноотропный препарат нового поколения от фармакологии до клиники // Ліки України. — 2002. — №3-4. — С. 1-8.
2. Нетрусова С.Г. Патогенетические и симптоматические составляющие клинических эффектов ноотропов // Ліки України. — №11.
3. Клименко В.Н., Беленичев И.Ф., Башкир И.Н. Медикаментозная защита головного мозга при выполнении операций на плечеголовных артериях // Клиническая хирургия. — 1993. — №7-8. — С. 14-16.
