Международный неврологический журнал 7 (45) 2011
Вернуться к номеру
Роль анксиолитиков в комплексном лечении хронических церебральных ишемий
Авторы: Морозова О.Г., Ярошевский А.А., Липинская Я.В., Харьковская медицинская академия последипломного образования
Рубрики: Неврология
Версия для печати
В статье рассматривается проблема когнитивных нарушений у пациентов с цереброваскулярными расстройствами. Представлены данные изучения эффективности анксиолитика этифоксина (Стрезам®) в комплексном лечении пациентов с гипертензивной дисциркуляторной энцефалопатией.
Цереброваскулярная патология, когнитивные нарушения, лечение, этифоксин.

Проблемы, связанные с хронической цереброваскулярной патологией, являются неотъемлемой частью обсуждений многих научных неврологических форумов. Качество жизни пациентов с хроническими церебральными ишемиями, снижение их трудовых, социальных и адаптационных возможностей вызывают сегодня не меньшее беспокойство, чем проблемы пациентов с острой цереброваскулярной патологией. В Украине сегодня не менее 3 млн человек страдают цереброваскулярными заболеваниями различной степени тяжести. За последние 10 лет темпы роста распространенности различных форм хронических сосудистых заболеваний мозга увеличились в 2 раза [9].
Снижение качества жизни при цереброваскулярной патологии кроме развития двигательных пирамидных, подкорковых, атактических синдромов связано с возникновением когнитивных расстройств. На сегодняшний день цереброваскулярные заболевания называются второй по частоте причиной развития приобретенного когнитивного дефицита, в том числе сосудистой деменции, а также играют значительную роль в развитии нейродегенеративных церебральных заболеваний, включая болезнь Альцгеймера [9, 15]. Термин «сосудистые когнитивные расстройства» (англ. vascular cognitive impairment) подразумевает сочетание факторов нарушения церебральной гемодинамики и развития нарушений таких когнитивных функций, как память, интеллект, праксис, гнозис, речь, внимание. Весомый вклад в развитие сосудистых когнитивных нарушений вносит хроническая церебральная ишемия, называемая в отечественной клинической неврологической практике дисциркуляторной энцефалопатией (ДЭ). ДЭ развивается на фоне артериальной гипертензии, атеросклероза и их сочетания и проявляется когнитивными, эмоциональными и объективными неврологическими синдромами (вестибулярно-атактическими, моторной, сенсорной недостаточностью, подкорковыми и др.). Неврологические, когнитивные и эмоциональные расстройства являются результатом структурных изменений головного мозга при дисциркуляторной энцефалопатии и составляют ядро клинической картины заболевания. В настоящей статье хотелось бы остановиться на двух облигатных синдромах ДЭ — когнитивной и эмоционально-аффективной дисфункции.
Коморбидность когнитивных и эмоциональных нарушений при хронической церебральной ишемии обсуждается многими исследователями, причем подчеркивается сложность и неоднозначность их взаимосвязи.
Такая взаимосвязь, по мнению многих авторов, обусловлена прежде всего анатомо-физиологическими особенностями развития церебральной дисциркуляции, особенно при артериальной гипертензии, в глубинных структурах мозга, приводящей к развитию феномена разобщения [9, 15, 18]. Эмоциональные нарушения не просто сочетаются с когнитивными, но и могут оказывать неблагоприятное влияние на когнитивную сферу. По мнению некоторых авторов, наличие эмоциональных нарушений способно усугублять выраженность когнитивных расстройств из-за повышения уровня тревоги и связанных с этим трудностей сосредоточения, неуверенности и ожидания неудачи [14, 16].
Так, результаты работы G. Grace и соавт. продемонстрировали влияние тревожных черт (но не депрессии) на результаты оценки памяти и скорости переработки информации, причем выраженность тревожных черт коррелировала с результатами исследования с расчетом индекса отсроченного воспроизведения шкалы памяти Векслера [21].
Влияние стресса на когнитивные функции опосредует передняя цингулярная кора (ПЦК) [16, 22]. В пределах ПЦК различают два отдела: аффективный и когнитивный. Аффективный отдел ПЦК связан с миндалиной, передним островком и орбитофронтальной корой и, таким образом, участвует в регуляции эмоцио-нального состояния. Когнитивный отдел ПЦК связан с такими структурами, как латеральная префронтальная кора, и, таким образом, участвует в регуляции функции внимания, выборе способа реагирования, рабочей памяти. ПЦК осуществляет функцию исполнительного внимания (переключение с одного задания на другое, распределение ресурсов внимания и др.) [16, 22]. Кроме того, ПЦК входит в корково-таламомезэнцефальную систему, которая участвует в процессе переключения внимания [21].
Считается, что ПЦК осуществляет исполнительный контроль ресурсов внимания в условиях эмоционального дистресса [15, 16]. Во время выполнения нейропсихологических тестов, требующих определенного эмоционального напряжения, происходит подавление активности когнитивного отдела ПЦК. Экспериментальным путем у здоровых было выявлено снижение активности когнитивного отдела при депрессивном состоянии и стрессе. Результаты функцио-нальной МРТ продемонстрировали при этом изменения в ПЦК [18].
Исходя из этого, можно предполагать, что дистресс может вызывать нарушения памяти. По-разному реагирует в зависимости от уровня тревоги и энторинальная кора гиппокампа, которая также ответственна за процессы памяти [22].
Таким образом, когнитивные и эмоционально-аффективные нарушения при ДЭ взаимосвязаны патогенетически и могут взаимоусиливать друг друга. Это прежде всего касается тревоги, которая особенно характерна для лиц с ДЭ 1-й стадии. Кроме того, как известно, тревога может осложнять течение сердечно-сосудистых заболеваний. Так, синдром тревоги негативно влияет на течение и прогноз всех видов кардиологической патологии, ухудшает ответ на фармакотерапию кардиотропными средствами, усложняет процесс ресоциализации больных [1, 2]. Результаты проспективных многолетних исследований с участием здоровых лиц выявили 3–4-кратное повышение риска развития кардиоваскулярных событий у пациентов с тревожным и тревожно-депрессивным расстройством [5, 6]. Оказалось, что психоэмоциональный дисбаланс коррелирует с более тяжелым течением соматического заболевания и 3-кратным увеличением смертности, в частности, от сердечной недостаточности [5, 6]. Сегодня считается доказанным, что синдром тревоги и тревожно-депрессивные расстройства являются предиктором смертности у пациентов с ишемической болезнью сердца [8].
Таким образом, подбор терапии пациентов, страдающих ДЭ, должен осуществляться с учетом двух главных синдромов — когнитивных и эмоциональных нарушений. При этом следует помнить, что назначаемые ноотропы, улучшая течение мнестических процессов, могут повышать уровень тревоги, а классические транквилизаторы (бензодиазепины) имеют побочные эффекты в виде подавления активности, ухудшения памяти, нарушения координации движения [13].
В связи с этим для коррекции эмоциональных расстройств нами был выбран анксиолитик этифоксин (Стрезам®, Biocodex, Франция), обладающий уникальным механизмом действия, выделяющим его среди всех других анксиолитиков [3, 17].
Цель исследования: изучение влияния анксиолитика этифоксина (Стрезам®) на эффективность терапии пациентов, страдающих гипертензивной дисциркуляторной энцефалопатией (ГДЭ) 1-й стадии.
Выбор этифоксина для коррекции эмоциональных расстройств у пациентов с хронической церебральной ишемией, а именно с ГДЭ 1-й стадии, с нашей точки зрения, обосновывается следующими положениями:
1. Действие этифоксина на тормозные процессы в центральной нервной системе следует рассматривать как наиболее физиологичное среди всех препаратов-анксиолитиков, сочетающее в себе селективность и одновременно политопность воздействия на разные звенья ГАМКергической нейротрансмиссии [3] (активация хлорного ионного канала — важнейшего компонента ГАМК-А-рецептора, и, соответственно, стимуляция ГАМКергических процессов [19, 24], что принципиально отличает его действие от анксиолитиков бензодиазепинового ряда; активирующее влияние на биосинтез нейростероидов, синтезирующихся в глиальных клетках и повышающих чувствительность ГАМК-А-рецепторов к ГАМК [23]), что обеспечивает большую выраженность и длительность противотревожного действия.
2. Этифоксин в многочисленных исследованиях (многоцентровые рандомизированные, двойные слепые плацебо-контролируемые, сравнительные) проявил себя как эффективное средство для коррекции психовегетативного синдрома, который на начальной стадии энцефалопатии является ведущим [4, 10, 20]. В рамках многочисленных клинических испытаний, выполненных в различных форматах, было доказано наличие у препарата Стрезам® выраженного анксиолитического действия, сопоставимого по силе с бензодиазепинами, в сочетании с вегетостабилизирующими свойствами и нормализацией сна на фоне общей стабилизации психоэмоционального состояния у пациентов с гипертонической болезнью, соматоформной вегетативной дисфункцией, расстройствами адаптации [3, 7, 11, 20].
3. Стрезам® в отличие от бензодиазепинов не оказывает негативного влияния на психомоторные и когнитивные функции, не вызывает вялости, сонливости, миорелаксации и т.д., в том числе у пожилых больных [3, 13], а также не проявляет каких-либо нежелательных соматотропных эффектов, что является важным при лечении пациентов, страдающих ДЭ.
Характеристика пациентов и методов исследования
Под нашим наблюдением находилось 38 пациентов с гипертензивной дисциркуляторной энцефалопатией 1-й стадии в возрасте от 39 до 47 лет (20 женщин, 18 мужчин). Диагноз верифицировался согласно протоколу «Надання медичної допомоги за спеціальністю «Неврологія» (Наказ № 487 МОЗ України) с помощью клинического неврологического осмотра, нейропсихологического исследования, изучения церебральной гемодинамики (УЗДГ), с учетом консультативных заключений терапевта или кардиолога (наличие артериальной гипертензии), а также данных нейровизуализации и исследования глазного дна.
В связи с наличием у всех пациентов вегетативной дисфункции было проведено тщательное изучение вегетативного гомеостаза с помощью субъективной и объективной вегетативных шкал (А.М. Вейн, 2000). Эмоциональные нарушения (количественная выраженность тревоги и депрессии) исследовались с помощью шкалы Гамильтона. Для определения выраженности когнитивных нарушений пациенты тестировались по шкале ММSE с отдельной оценкой внимания по методу отсчитывания чисел и кратковременной памяти [18]. Кроме того, исследовались внимание и слухоречевая память по А.Р. Лурия, а также использовались таблицы Шульте.
Статистическая обработка полученных результатов проводилась с помощью пакета прикладных программ Microsoft Exсel, Statistica (версия 6), с оценкой средних значений М, их ошибки n, критерия Стьюдента и достоверности статистических показателей p. Различия считались достоверными при р < 0,05.
У обследованных пациентов наблюдались следующие неврологические синдромы: цефалгический, вегетативной дисфункции, вестибулярно-атактический, пирамидных нарушений в виде повышения сухожильных рефлексов и анизорефлексии, легких стволовых дисфункций в виде нарушения зрачковых реакций и глазодвигательных расстройств, легкого когнитивного дефицита в виде нарушения внимания, забывчивости, снижения памяти, некоторой торпидности процессов удержания интеллектуальной нагрузки и уменьшения продуктивности запоминания, а также эмоциональных нарушений тревожного и тревожно-депрессивного характера.
В связи с этим согласно протоколу оправданным был выбор терапии, направленной на коррекцию сосудистых, когнитивных и эмоционально-аффективных нарушений у пациентов с ДЭ.
Для изучения влияния этифоксина на эффективность терапии пациентов, страдающих ГДЭ 1-й ст., пациенты методом случайной выборки были разделены на две группы, идентичные по полу и возрасту: 1-я группа — основная (23 пациента); 2-я группа — сравнения (15 пациентов). Обе группы пациентов получали антигипертензивную терапию под контролем артериального давления и вазоактивные препараты для улучшения церебральной гемодинамики. Первой группе пациентов дополнительно назначался Стрезам® по одной капсуле (150 мг) трижды в сутки в течение месяца. Контроль эффективности терапии осуществлялся через месяц и через три месяца после начала лечения. Результаты оценивали по динамике жалоб, неврологического и нейропсихологического исследований.
Результаты и их обсуждение
Исследование показало наличие когнитивных, эмоцио- нальных и вегетативных нарушений различной степени выраженности у пациентов обеих групп. Так, пациенты обеих групп предъявляли жалобы на сложности умственного сосредоточения (55 % больных), на проблемы с запоминанием информации (45 % больных). Согласно исследованию средний балл по шкале ММSE составил 26,90 ± 0,18. С помощью теста отсчитывания чисел в обеих группах в 100 % случаев выявлены быстрая утомляемость, снижение концентрации внимания, некоторое затруднение умственной деятельности. Наиболее часто встречались следующие варианты ошибок: ошибки в единицах при переходе через десяток при отсчитывании чисел (32,5 %), характерные для затруднения умственной деятельности; ошибки в десятках, свойственные пациентам с неустойчивым вниманием (39,5 %). У 45 % больных к окончанию тестирования возрастала длительность пауз, что свидетельствовало о повышенной утомляемости и истощаемости. Таким образом, при оценке нейропсихологического статуса было выявлена тенденция к нарушению памяти и воспроизведения, а также достоверное нарушение внимания и счета.
Имеющийся у всех пациентов синдром вегетативной дисфункции (достоверное увеличение фонового показателя теста А.М. Вейна по объективной и субъективной шкалам — 29,4 ± 2,0 и 25,25 ± 2,70 балла соответственно) проявлялся эмоциональными расстройствами, немотивированной тревогой, раздражительностью, общей слабостью, кардиалгическим, кардиосенестопатическим, цефалгическим, мышечно-тоническим синдромами.
Выраженность эмоциональных нарушений и тяжесть тревожно-депрессивной симптоматики определялись прежде всего структурой личности пациента и его реакцией на заболевание. Уровень личностной тревожности у пациентов обеих групп был охарактеризован как высокий (29,2 ± 3,0 балла). Это свидетельствовало о том, что больные ДЭ склонны воспринимать даже незначительные стрессовые и жизненные ситуации как угрожающие. Уровень депрессии у пациентов обеих групп был оценен по шкале Гамильтона как легкий.
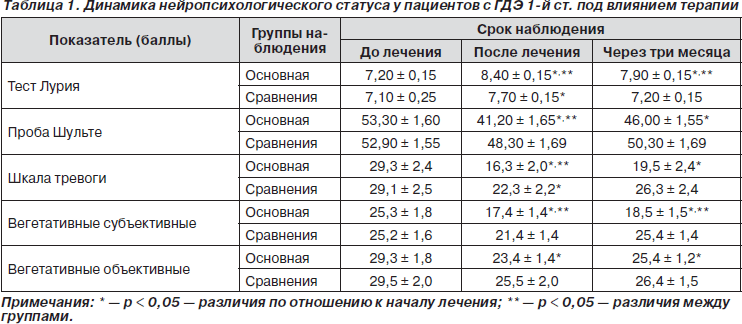
В результате проведенной терапии состояние пациентов обеих групп улучшилось относительно всех изуча- емых показателей, что свидетельствовало об участии церебральной дисциркуляции в патогенезе вегетативно-эмоциональных и когнитивных расстройств (табл. 1). Однако результаты терапии у пациентов основной группы были достоверно выше относительно тревожных, субъективных вегетативных и когнитивных расстройств.
Как следует из данных табл. 1, при лечении пациентов с использованием препарата Стрезам® через 30 дней наблюдения отмечалось достоверное уменьшение параметров, определяющих по шкале Гамильтона уровень тревожности. Снижение тревожности сопровождалось достоверным снижением выраженности вегетативных симптомов как по субъективной, так и по объективной шкалам, причем позитивный эффект сохранялся и в течение последующих двух месяцев, имея, однако, тенденцию к снижению. Очевидно, пациенты, страдающие ГДЭ, требуют более длительного (в течение двух-трех месяцев) приема анксиолитических препаратов. Данный эффект препарата Стрезам® явился достаточно прогнозируемым, и настоящее исследование подтвердило эффективность терапии у категории пациентов с хронической церебральной ишемией, развившейся на фоне артериальной гипертензии.
Более интересными, с нашей точки зрения, оказались результаты, касающиеся динамики когнитивных нарушений. Параллельно со снижением тревожности и нормализацией вегетативных показателей происходило улучшение показателей когнитивных. Причем данное улучшение на фоне комплексной терапии с использованием препарата Стрезам® было достоверно более высоким, чем позитивная динамика когнитивных функций при вазоактивной и антигипертензивной терапии.
Прежде всего на фоне терапии препаратом Стрезам® отмечалось достоверное уменьшение времени, затраченного пациентами на выполнение задания по таблицам Шульте (p < 0,05), тогда как у пациентов группы сравнения отмечалась лишь соответствующая тенденция, не достигающая уровня статистической значимости. Причем достоверная в начале лечения разница сохранялась и через три месяца, хотя время, затраченное на выполнение задания, увеличивалось.
Аналогичные результаты были получены при изучении теста Лурия по воспроизведению 10 слов. Показатель достоверно повышался на фоне лечения препаратом Стрезам® через месяц после начала терапии и несколько снижался через три месяца у пациентов основной группы, оставаясь достоверным относительно начала лечения, тогда как в группе сравнения показатели достоверно улучшались к концу курса терапии, а затем наступало ухудшение.
Таким образом, можно говорить об оптимизирующем влиянии препарата Стрезам® на внимание и мышление. Об этом свидетельствует тот факт, что на фоне приема препарата Стрезам® происходило сокращение общего времени выполнения пробы Шульте и количества совершаемых ошибок при пробах со слухоречевой памятью по А.Р. Лурия. Кроме того, это может свидетельствовать о сопряженности анксиолитического эффекта препарата Стрезам® с улучшением кратковременной памяти, хотя полученные данные требуют дальнейшего изучения.
Следует также отметить, что ни в одном случае при приеме препарата Стрезам® не наблюдалось побочных эффектов, препарат легко переносился и не требовал коррекции дозы.
Таким образом, результаты исследования могут свидетельствовать о патогенетической роли тревожных нарушений в клиническом оформлении хронических церебральных ишемий, в частности гипертензивной дисциркуляторной энцефалопатии, и их (тревожных нарушений) негативном влиянии на течение цереброваскулярной патологии. Подобные результаты о негативном влиянии синдрома тревоги на течение и прогноз всех видов патологии сердца получены в кардиологии [5, 6, 11, 12]. Кроме того, можно предполагать, что синдром тревоги ухудшает ответ на фармакотерапию вазоактивными препаратами, хотя подобное утверждение нуждается в дополнительном изучении.
Выводы
1. Применение анксиолитика этифоксина (Стрезам®) в комплексном лечении ГДЭ способствует повышению эффективности терапии в целом за счет уменьшения тревожности и вегетативной лабильности.
2. Использование в терапии хронической церебральной ишемии, развившейся на фоне артериальной гипертензии, анксиолитика Стрезам® приводило к более эффективной коррекции когнитивных нарушений.
3. Препарат Стрезам® по 150 мг трижды в сутки в течение 1–3 месяцев следует рекомендовать для повышения эффективности лечения пациентов, страдающих хронической церебральной ишемией, развившейся на фоне артериальной гипертензии.
1. Акарачкова Г.С., Шварков С.Б. Тревога в неврологической и общесоматической практике. Современные аспекты терапии // Рус. мед. журн. — 2007. — Т. 15, № 5. — С. 440-445.
2. Булдакова Н.Г. Психофармакотерапия в кардиологии // Рус. мед. журн. — 2006. — Т. 14, № 10. — С. 8-13.
3. Бурчинский С.Г. Стрезам (этифоксин) — новый подход к фармакотерапии тревожно-невротических состояний // Новости мед. и фарм. — 2006. — № 10. — С. 7-8.
4. Виничук С.М., Крылова В.Ю., Рогоза С.В. Тревожные расстройства с нарушением адаптации и методы их терапии // Междунар. неврол. журн. — 2008. — № 2. — С. 9-15.
5. Долженко М.Н. Психокардиология: применение анксиолитиков в лечении сердечно-сосудистых заболеваний // Therapia. — 2007. — № 10. — С. 35-40.
6. Ибатов И., Сыркин А., Вейн А. Тревога и ишемическая болезнь сердца // Врач. — 2003. — № 9. — С. 8-11.
7. Марута Н.А., Семикина Е.Е. Применение анксиолитической терапии в лечении соматоформной вегетативной дисфункции // Новости мед. и фарм. — 2008. — № 5. — С. 14-15.
8. Медведев В.Э., Троснова А.П., Добровольский А.В. Психофармакотерапия тревожных расстройств у больных с сердечно-сосудистыми заболеваниями // Журн. неврол. психиат. — 2007. — Т. 107, № 7. — С. 25-29.
9. Міщенко Т.С. Сучасна діагностика і лікування у неврології та психіатрії / За ред. Т.С. Міщенко, В.С. Підкоритова. — К.: ТОВ «Доктор-Медіа», 2008. — 624 с.
10. Морозова О.Г., Киреев И.В. Коррекция вегетативных и тревожных нарушений в практике врача-интерниста // Психиатрия и неврология. — 2007. — 215; Новости мед. и фарм. — 2007. — № 7. — С. 6-7.
11. Остроумова О.Д. Артериальная гипертензия и тревожные состояния // Кардиол. — 2002. — № 2. — С. 95-99.
12. Приходько В.Ю., Масленникова Н.А., Редько Л.А. Коррекция психосоматических расстройств в практике терапевта // Новости мед. и фарм. — 2008. — № 4. — С. 18-20.
13. Табеева Г.Р. Бензодиазепины: между риском и пользой // Неврол. журн. — 2008. — № 5. — С. 4-9.
14. Челышева И.А. Когнитивные и эмоциональные расстройства при дисциркуляторной энцефалопатии: Автореф. дис… д-ра мед. наук. — М., 2004.
15. Яхно Н.Н. Когнитивные расстройства в неврологической клинике // Неврологический журнал. — 2006. — Т. 11. — Приложение № 1. — С. 4-12.
16. Apkarian A.V. Human brain mechanisms of pain perception and regulation in health and disease / A.V. Apkarian, M.C. Bushnell, R.D. Treede, J.K. Zubieta // Eur. J. Pain. — 2004. — Vol. 9. — P. 463-484.
17. Girard C., Liu S., Cadepond F., Adams D., Lacroix C., Verleye M., Gillardin J.M. et al. Etifoxine improves peripheral nerve regeneration and functional recovery // Proc. Natl. Acad. Sci USA. — 2008. — 105(51). — 20505–10 / Epub. — 2008.
18. Folstein M.F. Mini-Mental State a practical guidefor grading the mental state of patients for the clinician // J. Psych. Res. — 1975. — Vol. 22. — P. 1037-1045.
19. Hamon A., Morel A., Hue B., Verleye M., Gillardin J.M. The modulatory effects of the anxiolytic etifoxine on GABA(A) receptors are mediated by the beta subunit // Neuropharmacology. — 2003. — 45(3). — 293-303.
20. Micallef J., Soubrouillard C., Guet F. et al. A double blind parallel group placebo controlled comparison of sedative and mnesic effects of etifoxine and lorazepam in healthy subjectes // Fundam. Clin. Pharmacol. — 2001. — V. 15. — P. 209-216.
21. McCracken L.M. Predicting complaints of impaired cognitive functioning in patients with chronic pain / L.M. McCracken, G.L. Iverson // J. Pain. Symptom Manage. — 2001. — Vol. 21, № 5. — P. 392-396.
22. McEwen B.S. Stress and hyppocampal plasticity / B.S. McEwen // Annu. Rev. Neurosci. — 1999. — Vol. 22. — P. 105-122.
23. Ugale R.R., Sharma A.N., Kokare D.M., Hirani K., Subhedar N.K., Chopde C.T. Neurosteroid allopregnanolone mediates anxiolytic effect of etifoxine in rats // Brain Res. — 2007. — 1184. — 193-201 / Epub. — 2007.
24. Rapin J.P. Etifoxine: a new antianxiety agent // Act. Innov. Med. — 2000. — № 68. — P. 10-13.
25. Schlichter R., Rybalchenko V., Poisbeau P. et al. Modulation of GABAergic synaptic transmission by the non-benzodiazepine anxiolytic etifoxine // Neuropharmacology. — 2000. — V. 39. — P. 1523-1535.