Международный неврологический журнал 5 (43) 2011
Вернуться к номеру
Лечение нарушений мозгового кровообращения с помощью Цефаворы®: многоцентровое исследование
Авторы: Schauerte W., Grunwald, Germany
Рубрики: Неврология
Версия для печати
Введение
Нарушения работы головного мозга и их лечение приобретают все большее значение в медицинской практике вследствие общего постарения населения. Один из двадцати человек среди тех, кому за 65, и один из пяти человек среди тех, кому за 80, страдают от данной патологии.
Наряду с дегенеративными процессами подобные проблемы часто возникают в результате церебровас-кулярных нарушений, которые, в свою очередь, являются следствием расстройств сердечно-сосудистой системы. По этой причине и вследствие возможности развития эффекта обкрадывания терапия подобных расстройств должна быть направлена не столько на то, чтобы усилить локальное кровообращение в мозге (вследствие локальной вазодилатации), сколько на общее улучшение системной и церебральной гемодинамики. В этом смысле была подтверждена эффективность препаратов, содержащих гинкго билобу, боярышник и омелу белую, особенно с учетом отсутствия у них побочных эффектов. Для того, чтобы еще глубже оценить эффективность и переносимость данных препаратов, было выполнено многоцентровое исследование, в рамках которого подобная терапия была назначена 804 пациентам с нарушением мозгового кровообращения.
Методы
Протокол исследования
В соответствии с протоколом настоящее открытое нерандомизированное многоцентровое исследование должно было быть выполнено с участием приблизительно 200 врачей, из расчета по 5 пациентов с нарушением мозгового кровообращения на каждого врача, в условиях повседневной амбулаторной практики и на фоне терапии сопутствующих заболеваний.
Проблемы с мозговым кровообращением в исходных условиях должны были быть охарактеризованы с помощью стандартизированного обследования, охватывающего головные боли, головокружение и нарушение памяти сосудистого генеза, колебания артериального давления, нарушения гемодинамики, жалобы на стенокардию и сведения о транзиторных ишемических атаках. Тяжесть нарушения мозгового кровообращения должна была быть квалифицирована с помощью специальной шкалы от «несущественной» до «легкой», «умеренной» или «выраженной» для таких симптомов, как головокружение, головная боль, звон в ушах, нарушение памяти и концентрации внимания, тревога, депрессия и расстройство сна. Для того чтобы оценить эффективность терапии в течение примерно 6 недель лечения, дозу тестируемого препарата, тяжесть нарушения мозгового кровообращения и регистрируемые побочные эффекты оценивали в двух контрольных точках — спустя примерно 3 и 6 недель. В добавок к этому во время последнего обследования (спустя примерно 6 недель) должна была быть оценена эффективность терапии (шкала: «нет симптомов», «отчетливое улучшение», «небольшое улучшение», «нет терапевтического эффекта») и ее переносимость (шкала: «очень хорошая», «хорошая», «средняя», «плохая»). Врач должен был также оценить комплайенс пациентов.
Исследуемый препарат и его доза
Цефавора® содержит 1,3 г гинкго билоба Æ, 2,7 г оме- лы белой Æ и 7,5 г боярышника Æ в 100 г препарата. Взрослые должны принимать 20–30 капель 3–4 раза в день.
Статистическая обработка
Перед шифрованием полученные документы должны были пройти проверку с помощью критерия правдоподобия и быть перепроверены после двойной независимой компьютерной обработки данных. Количественные характеристики, касающиеся пациентов, должны были быть описаны с помощью среднего арифметического значения, стандартного отклонения, минимума и максимума, первого и третьего квартиля, медианы.
Пациенты, демографические данные и диагноз
В исследование было включено 555 (69,0 %) женщин и 243 (30,2 %) мужчины. Пол не был указан у шести (0,7 %) пациентов. Возраст пациентов составил 67,0 ± 4,3 года, масса тела 72,1 ± 12,7 кг, средний рост 167,1 ± 7,9 см, средний индекс массы тела 25,8 ± ± 4,0 кг/м2. 15,4 % пациентов сообщили, что они курят сигареты; 10,5 % из некурящих пациентов сообщили, что они курили их ранее. У всех пациентов, кроме одного, наблюдались преимущественно три или четыре типичных симптома нарушения мозгового кровообращения. Наиболее частыми симптомами были приступы головокружения, нарушение памяти и нарушение гемодинамики. 543 пациента (67,5 %) страдали от нарушения мозгового кровообращения ранее, 256 пациентов (31,8 %) заболели впервые. Пациенты из первой упомянутой группы (531 чел.) сообщили, что они страдают данной патологией в среднем уже 4,1 ± 4,0 года. Из них 280 пациентов ранее уже получали препараты, усиливающие кровообращение (128 пациентов), противорвотные средства/средства против головокружения, антигипертензивные средства/блокаторы кальциевых каналов (24 пациента в каждом случае), сердечные/антиангинальные средства (21 пациент) и/или психофармакологические средства (15 пациентов). Кроме того, 580 пациентов сообщили о наличии сопутствующих заболеваний, для лечения которых 542 пациента получали до 5 различных препаратов. Наиболее часто требовали лечения заболевания сердечно-сосудистой, дыхательной и двигательной систем, соединительной ткани, эндокринной системы и обмена веществ. Наиболее часто применяемыми препаратами в составе сопутствующей терапии были антигипертензивные и сердечные средства (сообщили по 100 пациентов в каждом случае).
Результаты
Длительность терапии, дозы и эффективность
В общей сложности могли быть проанализированы данные о 804 пациентах. Наличие терапевтического эффекта оценивали в среднем спустя 23,1 ± 10,2 дня и спустя 47,6 ± 17,6 дня. В течение всего этого периода времени пациенты получали первоначально назначенную дозу препарата — 70,3 ± 21,0 капли в день. Медиана, первый и третий квартили составили 60, 60 и 90 капель в день. Максимальная доза составила 150 капель, минимальная — 10 капель в день.
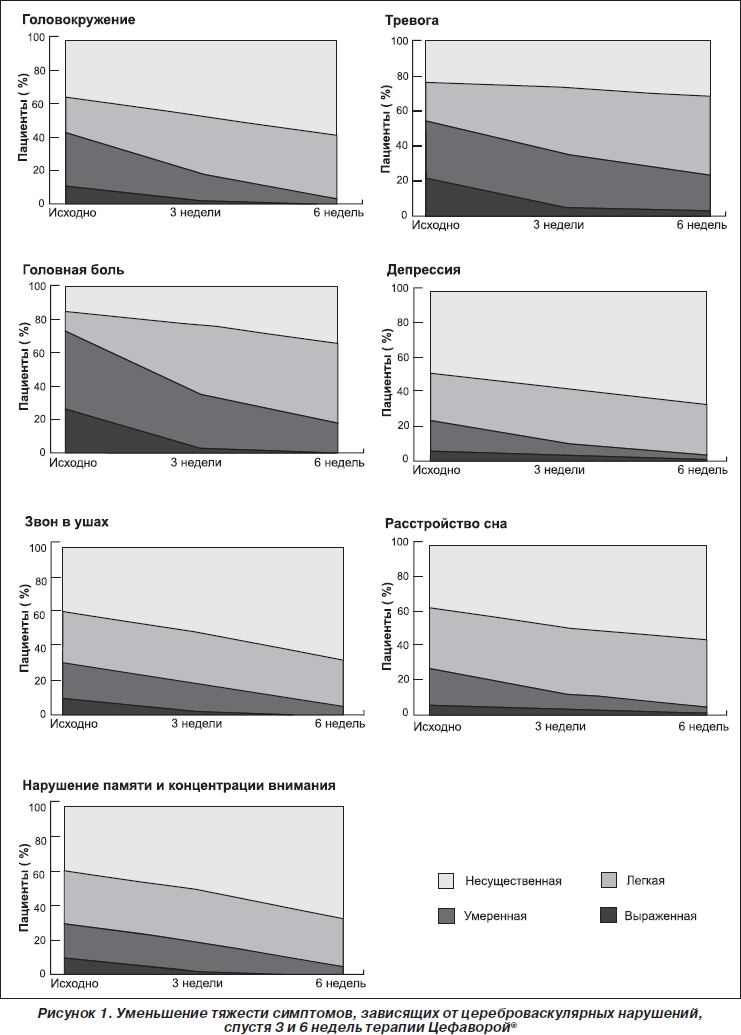
Во время лечения тяжесть цереброваскулярных симптомов, таких как головокружение, головная боль, звон в ушах, нарушение памяти и концентрации внимания, тревога, депрессия и расстройство сна, непрерывно уменьшалась (рис. 1). Фактически уже во время первой контрольной точки такая степень тяжести симптомов, как «выраженная», пациентами не называлась. В противоположность этому частота «несущественной» тяжести симптомов к моменту проведения финального оценивания увеличивалась вплоть до 60 %.
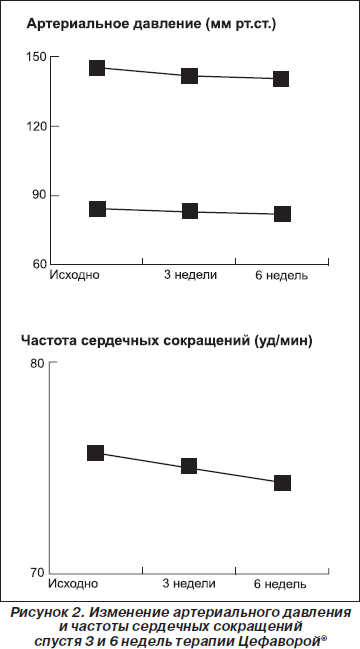
Одновременно систолическое и диастолическое артериальное давление и частота сердечных сокращений снижались с исходных цифр 145,0 ± 20,4 мм рт.ст., 84,2 ± 10,0 мм рт.ст. и 75,7 ± 9,2 уд/мин до 141,6 ± ± 18,4 мм рт.ст., 82,6 ± 9,2 мм рт.ст. и 75,1 ± 8,2 уд/мин во время первой контрольной точки и до 140,4 ± 16,9 мм рт.ст., 81,6 ± 8,4 мм рт.ст. и 74,3 ± 7,7 уд/мин во время финального оценивания (рис. 2).
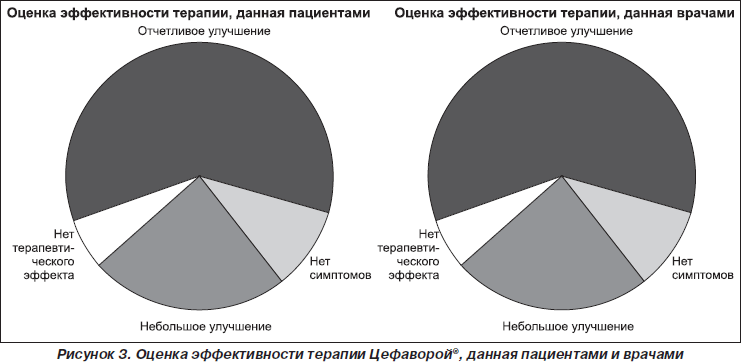
Финальное оценивание
В конце исследования врачи и пациенты давали более-менее одинаковые оценки эффективности (рис. 3) и переносимости терапии Цефаворой®. Спустя 6 недель терапии около 10 % пациентов сообщили, что у них симптомы полностью исчезли, около 60 % сообщили об отчетливом улучшении, 24 % — о небольшом улучшении, менее 5 % — об отсутствии терапевтического эффекта. При оценке врачами комплайенса у 634 пациентов было отмечено, что хороший комплайенс наблюдался у 78,9 % пациентов, средний — у 15,4 % пациентов и плохой — лишь у 2,1 % пациентов. Не сообщалось о развитии каких-либо нежелательных побочных эффектов. Соответственно, переносимость оценили как очень хорошую и хорошую более 95 % пациентов и врачей, а как плохую — только 0,2 %.
После завершения исследования 682 пациента (84,8 %) продолжили лечение тестируемым препаратом.
Обсуждение
Наиболее важными данными, полученными в ходе настоящего исследования, стало снижение частоты всех выраженных и умеренных цереброваскулярных жалоб и отсутствие каких-либо побочных эффектов в течение 6 недель исследования. Можно предположить, что наблюдаемое уменьшение частоты жалоб может быть связано с эффективностью тестируемого препарата.
Гомеопатический комбинированный препарат, использованный в нашем исследовании, не вызывал побочных эффектов. Это очень важно, поскольку исследованные нами пациенты имели большое количество сопутствующих заболеваний и принимали большое количество лекарственных средств для их лечения.
По этой причине более 95 % врачей и пациентов заявили о том, что Цефавора® имеет очень хорошую или хорошую переносимость. Менее благоприятная оценка, данная менее чем 5 % пациентов, соответствует таковой при применении плацебо-средств. Важно также, что препарат регулярно принимался (несколько раз в день) и после завершения исследования вследствие его хорошей переносимости и высокой эффективности препарат продолжили принимать 80 % пациентов. Вероятно, высокий комплайенс также вносил вклад в высокую эффективность препарата.
Следовательно, на практике было подтверждено, что тестируемый нами препарат практически лишен побочных эффектов, вследствие чего пациенты с большим желанием принимали его для эффективной терапии легких и умеренных цереброваскулярных нарушений.
Выводы
В многоцентровом нерандомизированном открытом исследовании была оценена эффективность и переносимость Цефаворы® (комбинированный препарат гинкго билобы, омелы белой и боярышника) в дозе 70 капель/день в условиях повседневной практики у 804 амбулаторных пациентов (преимущественно женщин — 69 %) с нарушением мозгового крово- обращения. Средний возраст пациентов составил 67,0 ± 14,3 года. В исходных условиях все пациенты (за исключением одного) сообщили о наличии по крайней мере одного из следующих цереброваскулярных симптомов: головных болей, головокружения или нарушений памяти сосудистого генеза, колебаний артериального давления, нарушений гемодинамики, жалоб на стенокардию или сведений о транзиторных ишемических атаках. У 256 пациентов нарушение мозгового кровообращения было выявлено впервые; 543 пациента сообщили о том, что они страдают от симптомов данной патологии в среднем в течение 4,1 ± 4,0 года.
В ходе исследования осуществляли мониторинг состояния пациентов — в начале лечения и спустя приблизительно 3 и 6 недель терапии.
Доза препарата оставалась неизменной в течение всего времени исследования. Систолическое и диастолическое артериальное давление снижалось со значений 145,0 ± 20,4 мм рт.ст. и 84,2 ± 10,0 мм рт.ст., зафиксированных в начале исследования, до значений 140,4 ± 16,9 мм рт.ст. и 82,6 ± 9,2 мм рт.ст., полученных в конце исследования. Частота сердечных сокращений снижалась соответственно с 75,7 ± 9,2 уд/мин до 74,3 ± 7,7 уд/мин. Во время лечения тяжесть таких симптомов, как головокружение, головная боль, звон в ушах, нарушение памяти и концентрации внимания, тревога, депрессия и расстройство сна, непрерывно снижалась. Во время финальной оценки эффективности лечения более 70 % врачей и пациентов ответили «нет симптомов» или «отчетливое улучшение».
Более 95 % пациентов и врачей оценили переносимость терапии как «очень хорошую» или «хорошую». Не было отмечено никаких побочных эффектов.
После завершения исследования 682 пациента (84,8 %) продолжили лечение Цефаворой®, 108 пациентов прекратили прием препарата — в основном по собственному желанию — вследствие отсутствия жалоб. Только 7 пациентов сообщили о недостаточной терапевтической эффективности препарата. Ни один пациент не назвал развитие нежелательных побочных эффектов в качестве причины прекращения терапии. Таким образом, в ходе исследования было показано, что протестированный комбинированный препарат хорошо переносится и эффективно уменьшает тяжесть симптомов, связанных с цереброваскулярной патологией.
Перевод к.м.н. А.В. Савустьяненко
Оригинал статьи опубликован в Der Bayerische Internist, 5/1996: 46-50
1. BGA-Aufbereitungsmonographien der Kommission D. BAnz. Nr. 190a vom 10.10.1985 und Nr. 217a vom 22.11.1985.
2. Boericke O.E. Homoopathische Mittel und ihre Wirkungen. — Verlag Grundlagen und Praxis, Leer, 1972.
3. Lorenz P.R. Therapie zerebraler Durchblutungsstorungen: Multizentrische Beobachtungsstudie // Zeitschrift fur Allgemeinmedizin. — 1993. — 69. — 352-355.
4. Wiesenauer M. Homoopathie fur Apotheker und Arzte. — Dr. Apotheker Verlag, Stuttgart, 1984-1996.