Международный неврологический журнал 3 (41) 2011
Вернуться к номеру
Сравнение комбинированной терапии НПВС и витаминами группы В с монотерапией НПВС при лечении люмбаго: результаты исследования DOLOR
Авторы: MIBIELLI M.A. (a, b); GELLER M. (a, c); COHEN J.С. (c); GOLDBERG S.G. (c); COHEN M.T. (d, e); NUNES C.P. (a, f); OLIVEIRA L.B. (f); da FONSECA A.S. (a, g);
a - Centro Universitario Serra dos Orgaos (UNIFESO);
b - Sociedade Brasileira de Ortopedia e Traumatologia, Rio de Janeiro, Brazil;
c - Universidade Federal do Rio de Janeiro (UFRJ), Rio de Janeiro, Brazil;
d - Centro Ortopedico Traumatologico (COTRAUMA);
e - Instituto Nacional de Traumatologia e Ortopedia (INTO), Rio de Janeiro, Brazil;
f - Instituto de Pos-Graducao Medica Carlos Chagas (ICC), Rio de Janeiro, Brazil;
g - Universidade Estadual do Rio de Janeiro (UERJ), Rio de Janeiro, Brazil
Рубрики: Неврология
Версия для печати
Цель исследования: оценить влияние витаминов В1, В6 и В12 на обезболивающую активность нестероидных противовоспалительных средств (НПВС) при лечении люмбаго.
Дизайн и методы исследования. В ходе настоящего рандомизированного двойного слепого контролируемого параллельно-группового клинического исследования пациенты получали перорально 2 раза в день либо комбинированную терапию НПВС и витаминами группы В (группа 1: НПВС 50 мг + тиамин 50 мг, пиридоксин 50 мг + цианокобаламин 1 мг), либо монотерапию НПВС в дозе 50 мг (группа 2). Период исследования длился максимум 7 дней. Если выраженное уменьшение боли наблюдалось раньше (значение визуальной аналоговой шкалы < 20 мм и удовлетворенность пациентов степенью уменьшения боли), то пациенты могли выбыть из исследования спустя 3 или 5 дней лечения. Все пациенты дали письменное информированное согласие на участие в исследовании.
Основные конечные точки исследования. Первичной конечной точкой исследования служило количество пациентов, у которых наблюдалось достаточное ослабление боли спустя 3 дня лечения.
Результаты. 372 пациента были случайно распределены в одну из двух групп лечения: 1-я группа (НПВС + витамины группы В) — 187 пациентов, 2-я группа (только НПВС) — 185 пациентов. Спустя 3 дня лечения статистически достоверно большее количество пациентов в 1-й группе (n = 87; 46,5 %) по сравнению со 2-й группой (n = 55; 29 %) выбыло из исследования вследствие выраженного уменьшения интенсивности боли (X2 = 12,06; р = 0,0005). Кроме того, в группе применения комбинированной терапии наблюдалось более выраженное уменьшение боли, улучшение мобильности позвоночника и функциональности пациентов. Профиль безопасности препаратов в обеих группах соответствовал ожидаемому профилю безопасности для НПВС.
Выводы. Комбинированная терапия НПВС и витаминами группы В превосходила монотерапию НПВС в отношении ослабления люмбаго спустя 3 дня лечения. Профиль безопасности достоверно не различался между двумя исследуемыми видами терапии.
Боль в нижней части спины, НПВС, люмбаго, пиридоксина гидрохлорид, тиамина мононитрат, цианокобаламин.
Введение
Боль в нижней части спины (БНЧС), или люмбаго, характеризуется болевым синдромом, мышечным напряжением или ригидностью, которые локализуются ниже реберных краев и выше нижних ягодичных складок, с наличием или без боли в ногах. Она может быть острой, а также принимать хроническое течение, если персистирует 12 недель или более [1].
БНЧС является пятой наиболее частой причиной всех посещений к врачу. В течение жизни БНЧС возникает у 60–80 % европейцев; распространенность тяжелых случаев составляет около 14 % [2, 3]. Приблизительно 25 % взрослых страдает от этого расстройства, и около одной трети из них сообщают о существенных ограничениях активности, включая неспособность выполнять работу вследствие персистирующих или рецидивирующих эпизодов БНЧС.
Лишь в небольшом количестве случаев БНЧС вызывается специфическими патологическими процессами, такими как рак, инфекции позвоночника, переломы, стеноз спинномозгового канала или грыжи межпозвоночных дисков, имеющие симптомное течение. Напротив, более чем у 85 % пациентов не удается обнаружить специфических заболеваний или нарушений позвоночника, поэтому БНЧС у них классифицируют как неспецифическую. БНЧС проявляется в виде сложного мышечно-скелетного болевого синдрома.
Современные руководства для лечения БНЧС в качестве пероральной терапии первой или второй линии рекомендуют использовать простые анальгетики (например, парацетамол) или нестероидные противовоспалительные средства (НПВС) [4]. Применение НПВС особенно показано при наличии сопутствующего воспалительного процесса.
В ряде исследований сравнили эффективность различных НПВС с плацебо при лечении острой БНЧС. В результате было сообщено об общем уменьшении выраженности боли на фоне активной терапии [10–13].
В экспериментальных исследованиях, посвященных изучению комбинации препаратов с фиксированными дозами, использованной в настоящем клиническом исследовании (витамины В1, В6 и В12 + НПВС), было показано наличие синергического взаимодействия витаминов и НПВС. В моделях воспаления и боли у крыс НПВС-индуцированная аналгезия потенцировалась одновременным введением комбинации витаминов группы В [14–16].
В более ранних двойных слепых рандомизированных клинических исследованиях сравнили обез-боливающую эффективность монотерапии НПВС и терапии комбинацией фиксированных доз НПВС и витаминов группы В у пациентов с БНЧС и заболеваниями позвоночника с болезненными дегенеративными изменениями. В этих исследованиях результаты обез-боливания были более выражены при использовании комбинации с фиксированными дозами препаратов. У статистически достоверно большего количества пациентов в группе, получавшей НПВС и витамины группы В, наблюдалось более раннее начало уменьшения выраженности боли по сравнению с группой, получавшей только НПВС [17–21].
Для того чтобы подтвердить и расширить ранее полученные данные, было выполнено настоящее проспективное рандомизированное клиническое исследование, в рамках которого оценили эффективность таблетированного препарата, содержащего НПВС в дозе 50 мг и витамины В1 (50 мг), В6 (50 мг) и В12 (1 мг), по сравнению с таблетированным препаратом, содержащим только НПВС в дозе 50 мг. В исследовании принимали участие пациенты с острыми эпизодами БНЧС, кратность приема препарата составила 2 раза в день.
Пациенты и методы исследования
Исследование было выполнено в соответствии с Хельсинкской декларацией, Руководством по надлежащей клинической практике (ICH Topic E6 1995) и Бразильским регуляторным законодательством (Resolucao 196/96 do Conselho Nacional de Saude). Исследование было одобрено местным Комитетом по биоэтике (университет UNIFESO) под номером 003/2004 и выполнено в соответствии с протоколом исследования в Hospital Universitario Constantino Otaviano — университетской клинике при университете UNIFESO в г. Рио-де-Жанейро, Бразилия. Пациенты также присылались из других центров, расположенных в Рио-де-Жанейро: Centro Ortopedico Traumatologico, Universidade Federal, Santa Casa de Misericordia и Hospital Souza Aguiar.
Пациенты
После того как протокол исследования был одобрен местным Комитетом по биоэтике, 372 пациента были рандомизированы к амбулаторному лечению. Критерии включения пациентов в исследование: возраст 18–65 лет; клиническая картина острого нетравматического люмбаго, длящегося не более 3 дней, с оценкой тяжести боли по визуальной аналоговой шкале (ВАШ) (0–100 мм) от 20 до 80 мм. Женщины фертильного возраста должны были пройти тест мочи на отсутствие беременности и осуществлять адекватную контрацепцию во время исследования. Все рандомизированные пациенты давали письменное информированное согласие на участие в исследовании.
Протокол исследования
В протоколе исследования было запланировано четыре визита в исследовательский центр: визит 1 — до начала лечения, включал скрининг, рандомизацию и исходное оценивание; визит 2 — через 3 дня лечения; визит 3 — через 5 дней лечения; визит 4 — через 7 дней лечения.
Скрининг пациентов во время первого визита осуществлялся путем проведения полного объективного и лабораторного обследования. Если пациент соответствовал критериям включения в исследование, врач присваивал ему трехзначный номер в соответствии с тем, каким по счету он прибыл в исследовательский центр.
Пациенты 1-й группы получали таблетки, содержащие 50 мг НПВС, 50 мг тиамина мононитрата (В1) и 1 мг цианокобаламина (В12). Пациенты 2-й группы получали таблетки, содержащие 50 мг НПВС. Оба вида таблеток были идентичны по размеру, форме, цвету и упаковке. Пациенты получали исследуемый препарат на следующие 3 дня плюс 1 день («на всякий случай»). Пациентов тщательно инструктировали выпивать одну таблетку во время завтрака и одну таблетку в обед. Спустя первые 3 дня лечения пациенты возвращались в исследовательский центр для выполнения запланированных тестов (визит 2), и при необходимости продолжить лечение им выдавали препарат на 2 следующих дня плюс 1 день («на всякий случай»). Все то же самое повторяли и во время визита 3. Во время каждого визита пациентов просили возвращать остатки исследуемого препарата и упаковку, что позволяло оценивать комплайенс (его определяли как количество принятых таблеток, разделенное на количество таблеток, которые должны были быть приняты, и умноженное на 100).
Если у пациента наблюдалось значительное уменьшение выраженности боли (по ВАШ < 20 мм и по субъективным ощущениям пациента) во время визита 2 и визита 3, он мог прекратить лечение после выполнения запланированных тестов. Любого пациента, у которого во время последнего визита (после которого лечение было прекращено) были выявлены побочные эффекты терапии, просили вернуться в исследовательский центр не позже чем через 10 дней. Если за это время осложнения не исчезали, пациента снова просили вернуться в исследовательский центр в течение последующих 10 дней. Так продолжалось до тех пор, пока осложнения не исчезали.
Оценка эффективности и переносимости
До начала лечения был собран медицинский анамнез (включая предыдущие случаи люмбаго, травмы позвоночника и оперативные вмешательства), выполнено полное объективное обследование и лабораторные тесты. В регистрационные карты пациентов до начала лечения была занесена следующая информация: дата рождения, пол, национальность, рост, вес, окружность талии, индекс массы тела, общий пищевой статус, употребление алкоголя, табакокурение, физический труд и занятия спортом. Лабораторные тесты, выполненные до начала лечения, включали подсчет форменных элементов крови, определение частичного тромбопластинового времени (ЧТВ), международного нормализованного отношения (МНО), тощакового уровня глюкозы, гликозилированного гемоглобина А (HbA1c), аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), гамма-глутамилтрансферазы, креатинина, креатининкиназы, мочевой кислоты, азота мочевины крови, скорости оседания эритроцитов (СОЭ) и теста мочи на беременность для пациенток женского пола.
Эффективность проводимой терапии определяли с помощью ВАШ, опросника функциональности пациентов (ОФП) и оценки мобильности позвоночника (измерение расстояния от пальцев до пола при сгибании туловища вперед — РПП). При работе с ВАШ исследователь просил пациента сделать вертикальную отметку на 100-миллиметровой линейке в форме для сбора данных в любом месте от 0 (нет боли) до 100 мм (очень выраженная боль). Результирующее значение оценивали как расстояние от левого края шкалы (0 мм) до отметки, поставленной пациентом.
При заполнении ОФП больные должны были дать ответ «да» или «нет» на 12 вопросов, касающихся выполнения их повседневных навыков. За каждый ответ «да» присваивался один балл. Общее количество баллов и баллы, касающиеся отдельных вопросов, сравнивали применительно к проводимым видам терапии во время каждого визита.
Для оценки однородности пациентов 1-й и 2-й групп в отношении клинического состояния БНЧС были применены тест Шобера и оценка выраженности симптома Ласега. Если симптом Ласега наблюдался во время визита 1 (что указывало на наличие грыжи межпозвоночного диска), то пациента не включали в исследование.
Во время измерения расстояния от пальцев до пола при сгибании туловища вперед пациента просили не отрывая ног от пола наклониться вперед как можно ниже с руками, вытянутыми вперед. Затем измеряли расстояние между средним пальцем пациента и полом и записывали полученное значение в сантиметрах.
Во время последующих визитов пациенты проходили полное объективное обследование, включая оценку жизненно важных показателей, мобильности позвоночника, значений ВАШ и ОФП, и лабораторные тесты (гемоглобин, гематокрит, эритроциты, лейкоциты, ЧТВ, МНО, уровень глюкозы натощак, АЛТ, АСТ, креатинин и СОЭ). Во время визита 2, 3 и 4 пациентов спрашивали, было ли уже достигнутое ослабление боли удовлетворительным. Если пациент отвечал «да», а значение ВАШ было меньше 20 мм, то считали, что ослабление боли было достаточным, и пациента выводили из исследования. Кроме того, если состояние пациента ухудшалось по сравнению с состоянием до лечения, то ведущий исследователь мог принять решение о выведении пациента из исследования вследствие неэффективности проводимого лечения.
По окончании исследования выполняли оценку следующих показателей: общая эффективность и переносимость лечения (оценивались врачом) и общий комплайенс (рассчитывался как количество принятых таблеток, разделенное на количество таблеток, которые должны были быть приняты, и умноженное на 100). Кроме того, регистрировалось состояние пациентов на момент окончания исследования.
Статистический анализ
Статистический анализ был выполнен в соответствии с заранее определенным планом анализа данных, записанным в протоколе исследования. В анализ включали всех пациентов, рандомизированных к лечению, которые принимали хотя бы одну дозу тестируемых препаратов.
Статистический анализ был выполнен с помощью BIAS [23, 24]. Различия между группами считали достоверными при p < 0,05. При сравнении первичных конечных точек исследования использовали U-критерий Вилкоксона — Уитни для непараметрических выборок.
При оценке вторичных конечных точек исследования использовали одногрупповой t-критерий Стьюдента для сравнения параметрических значений внутри одной группы, критерий Вилкоксона для сравнения непараметрических значений внутри одной группы, критерий Уэлша для сравнения параметрических выборок, которые могут иметь отличающиеся дисперсии, критерий Мантеля — Ханзеля (критерий хи-квадрат для сравнения данных, представленных в категориальной шкале) и критерий ранговой корреляции Спирмена.
Результаты
Демографические данные и исходное состояние пациентов во время визита 1
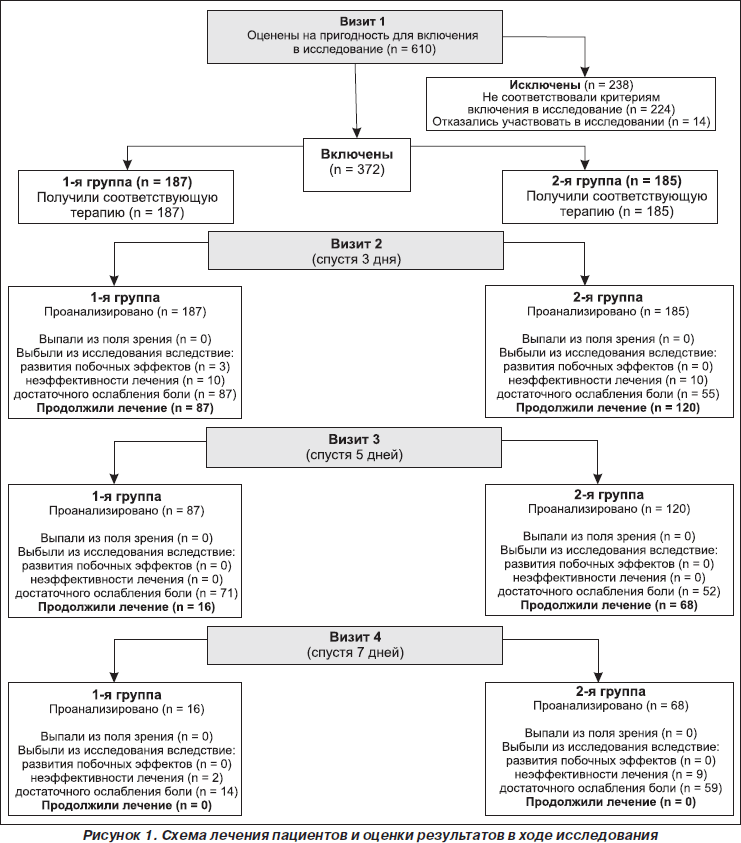
На рис. 1 представлено движение пациентов во время исследования. С сентября по декабрь 2007 г. в общей сложности скринингу подверглись 610 пациентов, из которых 372 были случайно распределены к одному из следующих видов лечения: НПВС + витамины группы В — 1-я группа (n = 187); только НПВС — 2-я группа (n = 185).
238 пациентов были исключены из исследования, поскольку они либо не соответствовали критериям включения в настоящее исследование (n = 224), либо отказались от участия в нем (n = 14).
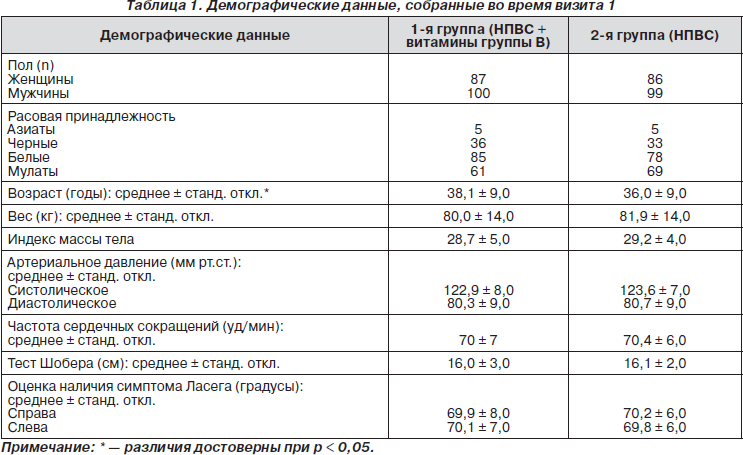
Демографические данные пациентов представлены в табл. 1. Что касается возраста пациентов, то между группами наблюдались достоверные различия в 2,05 года (р = 0,03; 95% ДИ 0,2–3,9), в то время как медиана возраста была равна 37 годам в обеих группах. Результаты теста Шобера и оценки выраженности симптома Ласега свидетельствуют о том, что клиническое состояние БНЧС в обеих группах было одинаковым.
Среднее значение ВАШ в 1-й группе составляет 48,0 ± 12,0 мм, а во 2-й группе — 52,6 ± 12,0 мм (D: в среднем 3,7 мм). До начала лечения наблюдались также небольшие различия между обеими группами при измерении расстояния от пальцев до пола при сгибании туловища вперед: 1-я группа — 19,6 ± 6,0 см, 2-я группа — 21,2 ± 6,0 см (D: в среднем 1,6 см). Сумма баллов по ОФП в 1-й группе (среднее значение 9; 4–12) соответствовала таковой во 2-й группе (среднее значение 9; 5–12). Во время визита 1 выраженность боли (ВАШ, мм) коррелировала с расстоянием от пальцев до пола при сгибании туловища вперед (см) (в 1-й группе коэффициент корреляции Спирмена R = 0,34, 95% ДИ 0,2–0,48; во 2-й группе коэффициент R = 0,56, 95% ДИ 0,2–0,48). Аналогичная корреляция наблюдалась между выраженностью боли (ВАШ) и значениями ОФП (в 1-й группе коэффициент корреляции Спирмена R = 0,39, 95% ДИ 0,256–0,52; во 2-й группе коэффициент R = 0,41, 95% ДИ 0,27–0,48).
Оценка эффективности лечения
Первичная конечная точка исследования — окончание лечения во время визита 2
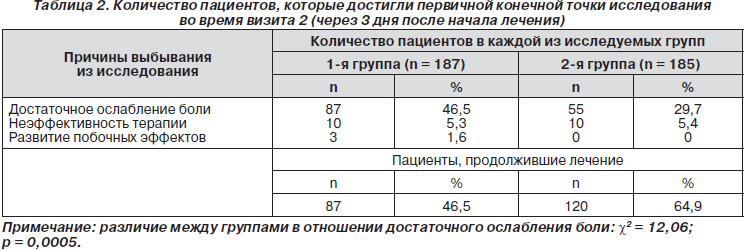
Оценка результатов лечения спустя 3 дня лечения (визит 2) представлена в табл. 2. Данные свидетельствуют о том, что 46,5 % пациентов в 1-й группе выбывало из исследования вследствие достаточного ослабления боли, в то время как во 2-й группе таких пациентов было только 29,7 %; разница между группами статистически достоверна и составляет 16,8 % (c2 = 12,32; p = 0,0005).
Вторичные конечные точки исследования — окончание лечения во время визита 3 и визита 4
Во время визита 3 (спустя 5 дней лечения) 123 из 207 пациентов выбыли из исследования вследствие достаточного уменьшения боли.
Как и во время визита 2, во время визита 3 в 1-й группе большее количество пациентов выбыло из исследования вследствие достаточного уменьшения выраженности боли (71/87; 82 %) по сравнению со 2-й группой (52/120; 43 %) (c2 = 30,6; p < 0,000; 95% ДИ 0,26–0,5). Ни один из пациентов во время визита 3 не выбыл из исследования вследствие усиления боли или развития побочных эффектов.
Во время визита 4 (спустя 7 дней лечения) 14 из 16 пациентов, остававшихся в 1-й группе (87,5 %), закончили исследование с достаточным ослаблением боли, у 2 пациентов лечение оказалось неэффективным (12,5 %). Аналогично из 68 пациентов, остававшихся во 2-й группе после визита 3, 59 пациентов (86,76 %) закончили исследование с достаточно выраженным уменьшением боли, у 9 пациентов (13,23 %) лечение было неэффективным. Доля пациентов, закончивших исследование во время визита 4 с достаточным ослаблением боли или с неэффективностью лечения, не различалась между группами.
Значения ВАШ — визит 2
Средние значения ВАШ во время визита 2 в 1-й группе составили 24,5 ± 20,0 мм, во 2-й группе — 31,9 ± 20,0 мм (p = 0,0003; D = –7,5; 95% ДИ от –11,5 до –3,4).
Среди пациентов, которые продолжили исследование дальше, значения ВАШ также достоверно различались в пользу 1-й группы (1-я группа — 33,6 ± 10,0 мм, 2-я группа — 38,3 ± 9,0 мм; р = 0,001; 95% ДИ от –7,4 до –2,1).
Спустя 3 дня лечения интенсивность боли уменьшалась в обеих исследуемых группах.
Среднее снижение значений ВАШ во время визита 2 в 1-й группе составило 24,5 ± 18,0 мм (р = 0,04; 95% ДИ 21,9–27,0), во 2-й группе — 20,7 ± 18,0 мм (р = 0,06; 95% ДИ 18,1–23,4). Различия между двумя группами были статистически достоверными (р = 0,044; 95% ДИ 0,08–7,4).
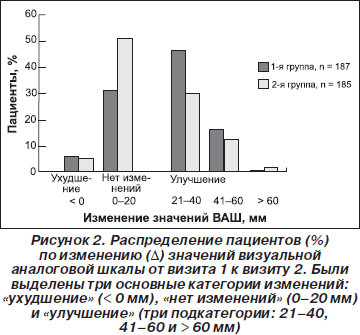
Лечение фиксированной комбинацией НПВС и витаминов группы В (1-я группа) обусловило улучшение значений ВАШ у большего количества пациентов (63,1 %) по сравнению с монотерапией НПВС (2-я группа; 43,8 %).
При объединении изменений значений ВАШ от визита 1 к визиту 2 в три основных категории (см. горизонтальную ось на рис. 2) улучшение наблюдалось в 1-й группе (рис. 2).
Значения ВАШ — визит 3
К визиту 3 среднее значение ВАШ у оставшихся в исследовании 207 пациентов продолжало снижаться. У 72 пациентов (82,8 %) в 1-й группе значения ВАШ были менее 20 мм. Во 2-й группе у 53 пациентов из 120 (44,1 %) значения ВАШ были ниже 20 мм. Различия между группами по количеству пациентов с достаточным ослаблением боли были достоверными (p < 0,001). Среднее значение ВАШ в 1-й группе составило 12,9 ± 10,0 мм, во 2-й группе — 20,1 ± 12,0 мм.
Расстояние от пальцев до пола при сгибании туловища вперед
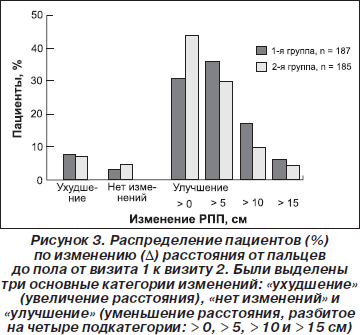
Через 3 дня лечения РПП снижалось в 1-й группе на 5,6 ± 6,0 см (p < 0,005; 95% ДИ 5,1–6,6), во 2-й группе — на 4,6 ± 6,0 см (p < 0,001; 95% ДИ 3,7–5,4), что привело к формированию среднегрупповой разницы величиной в 2,9 см (1-я группа — 13,7 ± 7,0 см, 2-я группа — 16,6 ± 7,0 см; р = 0,0001; 95% ДИ от –4,4 до –1,5). Достоверно более высокий процент пациентов в 1-й группе достигал лучших результатов (c2 = 3,86; p < 0,05) по сравнению со 2-й группой (рис. 3). Данное улучшение мобильности позвоночника прямо коррелировало со снижением интенсивности боли (ВАШ). Средняя разница РПП во время визита 3 между двумя группами лечения составила 3 см (p < 0,001; 95% ДИ от –4,4 до –1,5).
Опросник функциональности пациентов
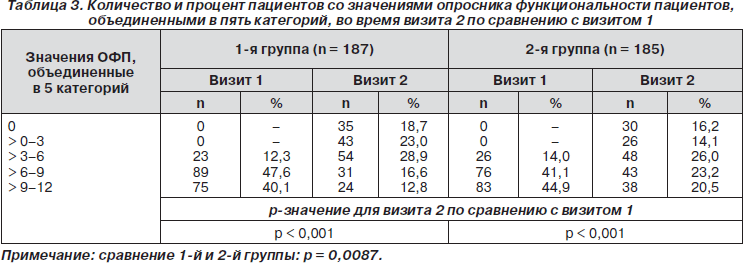
Количество пациентов с достоверными изменениями значений ОФП спустя 3 дня лечения представлено в табл. 3.
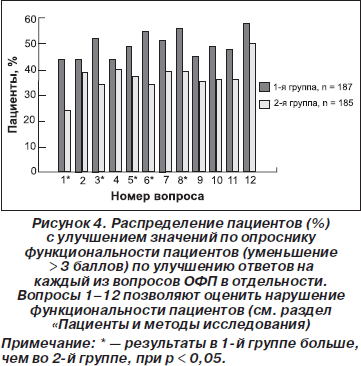
На рис. 4 представлен процент пациентов с улучшением по каждому из вопросов ОФП в отдельности во время визита 2. Улучшение функциональности коррелировало со снижением значений ВАШ в обеих группах. По ряду вопросов, касающихся мобильности позвоночника, улучшения были более выражены в 1-й группе (p < 0,05).
Безопасность и побочные эффекты
Побочные эффекты регистрировали во время каждого визита в течение всего периода лечения. Распределение побочных эффектов в ходе исследования представлено в табл. 4. У ряда пациентов наблюдалось несколько побочных эффектов.
В 1-й группе 3 пациента выбыли из исследования во время визита 2 вследствие транзиторного повышения уровня трансаминаз (n = 2) и диспепсии (n = 1).
Побочные эффекты, зафиксированные во время периода лечения, следует расценивать как типичные при назначении НПВС.
В ходе исследования не наблюдалось клинически достоверных различий между группами в отношении жизненно важных показателей. В обеих группах во время каждого визита средние значения лабораторных тестов находились в пределах нормы. Ни в один из визитов статистически достоверных различий по сравнению с исходными (до лечения) значениями не было.
Обсуждение
Основные сведения о дизайне и результатах исследования
Результаты нашего исследования свидетельствуют об усилении обезболивающего эффекта НПВС в комбинации с витаминами В1, В6 и В12, что подтверждает и расширяет данные предыдущих исследований [17–21] о том, что анальгетический эффект НПВС потенцируется витаминами группы В, при этом параллельно улучшается выполнение двигательных функций. Таким образом, наши данные и данные предыдущих исследований подтверждают вклад витаминов группы В в обезболивание при острой БНЧС.
Очевидно, что самым главным преимуществом для пациентов в нашем исследовании была более короткая длительность и меньшая выраженность боли при применении НПВС в сочетании с витаминами группы В, что очень важно для оценки качества жизни самими пациентами. И хотя мы не занимались этим в нашей работе, в предыдущих эпидемиологических исследованиях была особо подчеркнута значимость способности пациентов посещать работу. Снижение боли вместе с улучшением ОФП, наблюдаемое в настоящем исследовании, несомненно, будет вносить вклад в способность пациентов выполнять работу и другую деятельность.
Еще одно преимущество от сочетанного назначения витаминов группы В заключается в потенциальном снижении потребления НПВС. Имеется много данных о двух типах характерных побочных эффектов при назначении НПВС — риске развития желудочно-кишечных [31] и сердечно-сосудистых заболеваний [30]. Риск развития побочных эффектов растет при увеличении дозы и длительности приема этих препаратов. Следовательно, любое средство, которое может обусловить уменьшение дозы и длительности приема НПВС, способно вносить вклад в снижение частоты развития упомянутых осложнений.
Таким образом, сочетанное назначение витаминов группы В может помочь снизить риск развития потенциально тяжелых побочных эффектов, связанных с назначением НПВС. В ходе нашего исследования сочетанное назначение витаминов группы В и НПВС не приводило к росту частоты побочных эффектов (табл. 4). Однако, чтобы попытаться обнаружить статистически достоверное снижение частоты побочных эффектов при данном режиме терапии, требуется включение в исследование большего количества пациентов.
Результаты настоящего крупного исследования (372 пациента) не только согласуются с результатами ранее выполненных исследований [17–21], но и расширяют их данными о динамике функциональности пациентов, которая отражает их способность выполнять повседневную деятельность.
Важно, что все тесты, характеризующие достаточное ослабление боли у пациентов, были выполнены в одном университетском центре, что исключает наличие межцентровой вариации и увеличивает надежность настоящего исследования.
Ограничением исследования является его дизайн, поскольку не была предусмотрена ежедневная оценка ВАШ, что позволило бы получить непрерывную динамику интенсивности боли от начала до конца исследования.
Механизмы развития боли в нижней части спины
Несмотря на то что боль в нижней части спины является одной из наиболее частых жалоб в учреждениях первичного звена здравоохранения, ее этиология и патогенез все еще до конца не выяснены. В последние годы значительно расширились наши представления о разнообразных ноцицептивных, воспалительных, нейропатических и травматических/механических стимулах, которые могут вносить вклад в патофизиологию БНЧС. Например, в формирование поясничной боли могут вносить вклад механические причины, связанные с опорно-двигательной системой, что приводит к появлению ноцицептивной боли. Однако в то же самое время может наблюдаться раздражение или повреждение нервной системы, что также будет вносить вклад в формирование поясничной боли, вызывая нейропатическую боль [35]. Поликомпонентность БНЧС наблюдается очень часто, поэтому недавно в отношении нее была предложена концепция и термин «боль смешанной этиологии» [26]. Бороться с патогенетически смешанной ноцицептивной и нейропатической болью будет намного проще, если оптимизировать терапию так, чтобы она учитывала вовлечение этих различных механизмов в формирование боли. По-видимому, комбинированная терапия НПВС и витаминами группы В подтверждает это положение.
Широко известно, что ноцицептивная и воспалительная боль чувствительна к НПВС как в моделях на животных, так и у пациентов. Витамины группы В проявляют антиноцицептивное действие в отношении ноцицептивной/воспалительной боли как при использовании в виде монотерапии, так и в комбинации с НПВС [14–16]. Кроме того, было показано, что они тормозят аллодиническое поведение у крыс после перевязки спинномозговых нервов [27]. Аллодиния является выражением нейропатической боли гиперчувствительного типа у животных и человека. В моделях на крысах с перевязкой нервов или их перерезкой аллодиния сильно подавляется витаминами В1 и В12 и в меньшей степени — витамином В6.
Таким образом, витамины В1 и В12 являются сильными ингибиторами аллодинии в моделях нейропатической боли у крыс. Ряд фармакологических механизмов, не связанных с пищевой потребностью витаминов В, был предложен для того, чтобы объяснить их антиаллодиническое/обезболивающее действие. К ним относят активацию гуанилатциклазных путей [27] и восстановление Na+ тока в малых нейронах спинномозговых ганглиев, поврежденных компрессионно [32]. Нужно отметить, что НПВС, назначаемые крысам с аллодинией, не потенцирует антиаллодинические эффекты витаминов группы В и не вызывает антиаллодинический эффект при назначении в виде монотерапии [28]. Эти данные согласуются с неэффективностью НПВС при нейропатической боли, наблюдаемой у человека.
Таким образом, обезболивающий эффект НПВС направлен в основном против ноцицептивной/воспалительной боли, в то время как витамины группы В более склонны подавлять процессы, вовлеченные в нейропатическую боль. Принимая во внимание различные механизмы действия этих двух препаратов, мы полагаем, что рост обезболивающей активности при использовании комбинации НПВС/витаминов группы В, наблюдаемый в нашем исследовании, свидетельствует о том, что у большинства, если не у всех, наших пациентов БНЧС носит смешанный характер. Следовательно, НПВС и витамины группы В могут проявлять синергизм при лечении боли в нижней части спины. Необходимо проводить дальнейшие экспериментальные и клинические исследования, чтобы расширить данные, полученные в ходе настоящего исследования.
Представляется весьма интересным оценить полученные данные у пациентов с хронической БНЧС, что позволит глубже изучить механизмы нейропатической боли [26, 29].
Выводы
У 372 исследованных пациентов обезболивающая активность комбинации НПВС и витаминов В1, В6, В12 была выше по сравнению с монотерапией НПВС: уже через 3–5 дней лечения отмечалось более выраженное уменьшение боли. Поскольку БНЧС является многогранным синдромом, назначение только НПВС может не обеспечить достаточный обезболивающий эффект или потребовать более длительного времени лечения, чтобы достичь желаемого результата. В то же время комбинация НПВС с витаминами группы В обладает большей эффективностью, укорачивая время лечения и таким образом потенциально снижая риск развития побочных эффектов.
Перевод к.м.н. А.В. САВУСТЬЯНЕНКО
Печатается в сокращении
Оригинал статьи опубликован в журнале
Current Medical Research & Opinion. — 2009 Nov. — Vol. 25, № 11
1. Van Tulder M.W., Koeg B.W. Low back pain and sciatica // Clin. Evid. — 2001. — 6. — 0-19.
2. Breivik H., Callett B., Ventafridda V. et al. Survey of chronic pain in Europe: prevalence, impact on daily life, and treatment // Eur. J. Pain. — 2006. — 10. — 287-333.
3. Manek N., MacGregor A.J. Epidemiology of low back disorders // Curr. Opin. Rheumatol. — 2005. — 17(2). — 134-40.
4. European Guidelines for the management of acute non-specific low back pain in primary care // Eur. Spine J. — 2006. — 15 (Suppl. 2). — 169-91.
5. Sweetman S.C. Martindale: The Complete Drug Reference. — 35th ed. — London: Pharmaceutical Press, 2007.
6. Brune K., Hinz B. Nichtopioidanalgetika // Zenz B., Jurna I., Lehrbuch der Schmerztherapie. 2. Aufl. — Sttgt: Wiss-Verlag-Ges, 2001; ISBN 3-8047-1805-1.
7. Hinz B., Brune K. Schmerztherapie mit antipyretischen Anal-getika // Der Orthopдde. — 2007. — 36. — 23-31.
8. Steinmeyer J., Konttinen Y.T. Oral treatment options for degenerative joint disease — present and future // Adv. Drug Deliv. Rev. — 2006. — 58. — 168-211.
9. Ortiz M.I., Castaneda-Hernandez G., Rosas R. et al. Evidence for a new mechanism of action of diclofenac: activation of K+ channels // Proc. West Pharmacol. Soc. — 2001. — 44. — 19-21.
10. Van Tulder M.W., Scholten R.J.P.M., Koes B.W. et al. Nonsteroidal anti-inflammatory drugs for low back pain // Spine. — 2000. — 19. — 2501-13.
11. Koes B.W., van Tulder M.W., Peul W.C. Diagnosis and treatment of low back pain // BMJ. — 2006. — 332. — 1430-4.
12. Roelofs P.D.D.M., Deyo R.A., Koes B.W., Scholten R.J.P.M., van Tulder M.W. Nonsteroidal anti-inflammatory drugs for low back pain // Cochrane Database of Systematic Reviews 2008, Issue 3. DOI: 10.1002/14651858. CD000396.pub3.
13. Strumpf M., Linstedt U., Wiebalek A. et al. Medikamentцse Therapie bei Rьckenschmerzen // Schmerz. — 2001. — 15(6). — 453-60.
14. Bartoszyk G.D., Wild A. B-vitamins potentiate the antinociceptive effect of diclofenac in carrageenin-induced hyperalgesia in the rat tail pressure test // Neurosci. Lett. — 1989. — 101. — 95-100.
15. Reyes-Garcia G., Medina-Santillan R., Teran-Rosales F. et al. Characterization of the potentiation of the antinociceptive effect of diclofenac by vitamin B complex in the rat // J. Pharmacol. Toxicol. Meth. — 1999. — 42(1). — 73-7.
16. Rocha-Gonzбlez H.I., Terбn-Rosales F., Reyes-Garcнa G. et al. B vitamins increase the analgesic effect of diclofenac in the rat // Proc. West Pharmacol. Soc. — 2004. — 47. — 84-7.
17. Brьggemann G., Koehler C.O., Koch E.M.W. Ergebnisse einer Doppelblindprьfung Diclofenac + Vitamin B1, B6, B12 versus Diclofenac bei Patienten mit akuten Beschwerden im Lendenwirbelsaьlenbereich // Klin. Wochenschr. — 1990. — 68. — 116-20.
18. Kuhlwein A., Meyer H.J., Koehler C.O. Reduced need for diclofenac with concomitant B-vitamin therapy: results of a double-blind clinical study with reduced diclofenac-dosage (75 mg diclofenac vs. 75 mg diclofenac plus B-vitamins daily) in patients with acute lumbago // Klin. Wochenschr. — 1990. — 68. — 107-15.
19. Vetter G., Brьggemann G., Lettko M. et al. Verkьrzung der Diclofenac-Therapie durch B-Vitamine. Ergebnisse einer randomisierten Doppelblindstudie, Diclofenac 50 mg gegen Diclofenac 50 mg plus B-Vitamine, bei schmerzhaften Wirbelsдulenerkrankungen mit degenerativen Verдnderungen // Z. Rheumatol. 1988. — 47. — 351-62.
20. Koch E.M.W., Ehrhardt A. Der Beitrag von B-Vitaminen in der Therapie von Wirbelsaдlensyndromen // Rietbrock N. (Hrsg.). Pharmakologie und klinische Anwendung hochdosierter B-Vitamine. — Darmstadt: Steinkopff Verlag, 1991.
21. Lettko M. Ergebnisse einer Doppelblindstudie, Diclofe-nac und B-Vitamine gegen Diclofenac, zur Prьfung der additiven Wirksamkeit der B-Vitamine // Rheuma, Schmerz & Entzьndung. — 1986. — 8. — 22-30.
22. Langmann M.J., Weil J., Wainwright P. et al. Risks of bleeding peptic ulcer associated with individual non-steroidal anti-inflammatory drugs // Lancet. — 1994. — 343. — 1075-8.
23. Ackermann H. Biometrische Analayse von Stichproben (BIAS), Version 8.4; 2008-08-16 Epsiilon Verlag, Hochheim Darmstadt.
24. Sachs L. Angewandte Statistik. 7. Auflage. — Heidelberg: Springer Verlag, 1992; ISBN 3-540-52085-6.
25. Audette J.F., Emenike E., Meleger A.L. Neuropathic low back pain // Curr. Pain Headache. Rep. — 2005. — 9. — 68-77.
26. Baron R., Binder A. Wie neuropathisch ist die Lumboischialgie? // Der Orthopдde. — 2004. — 33. — 568-75.
27. Caram-Salas N.L., Reyes-Garcia G., Medina-Santilan R. et al. Thiamin and cyanocobalamin relieve neuropathic pain in rats // Pharmacology. — 2006. — 77(2). — 53-62.
28. Granados-Soto V., Sбnchez-Ramirez G., la Torre M.R. et al. Effect of diclofenac on the antiallodynic activity of vitamin B12 in a neuropathic pain model in the rat // Proc. West Pharmacol. Soc. — 2004. — 47. — 92-4.
29. Freynhagen R., Baron R., Tцlle T. et al. Screening of neuropathic pain components in patients with chronic back pain associated with nerve root compression: a prospective observational pilot study (MIPORT) // Curr. Med. Res. Opin. — 2006. — 22. — 529-37.
30. McGettigan P., Henry D. Cardiovascular risk and inhibition of cyclooxygenase: a systematic review of the observational studies of selective and nonselective inhibitors of cyclooxygenase 2 // JAMA. — 2006. — 296. — 1633-44.
31. Singh G., Triadafilopoulos G. Epidemiology of NSAID induced gastrointestinal complications // J. Rheumatol. Suppl. — 1999. — 56. — 18-24.
32. Song X.S., Huang Z.J., Song X.J. Thiamine suppresses thermal hyperalgesia, inhibits hyperexcitability, and lessens alterations of sodium currents in injured, dorsal root ganglion neurons in rats // Anesthesiology. — 2009. — 110. — 387-400.